题目内容
【题目】下列叙述中,不能用勒夏特列原理解释的是( )
A.红棕色的NO2,加压后颜色先变深后变浅
B.高压比常压有利于合成NH3的反应
C.由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深
D.黄绿色的氯水光照后颜色变浅
【答案】C
【解析】
A. NO2气体中存在2NO2![]() N2O4,增大压强,缩小容器的体积,气体浓度增大,即气体颜色加深,增大压强,平衡向正反应方向进行,N2O4为无色气体,即气体颜色变浅,可以用勒夏特列原理解释,故A不符合题意;
N2O4,增大压强,缩小容器的体积,气体浓度增大,即气体颜色加深,增大压强,平衡向正反应方向进行,N2O4为无色气体,即气体颜色变浅,可以用勒夏特列原理解释,故A不符合题意;
B. 合成氨气:N2(g)+3H2(g) ![]() 2NH3(g),增大压强,平衡向正反应方向进行,可以用勒夏特列原理解释,故B不符合题意;
2NH3(g),增大压强,平衡向正反应方向进行,可以用勒夏特列原理解释,故B不符合题意;
C. H2和I2反应H2(g)+I2(g) ![]() 2HI(g),增大压强平衡不移动,增大压强缩小容器的体积,组分浓度增大,则气体颜色变深,不能用勒夏特列原理解释,故C符合题意;
2HI(g),增大压强平衡不移动,增大压强缩小容器的体积,组分浓度增大,则气体颜色变深,不能用勒夏特列原理解释,故C符合题意;
D.氯水中存在:Cl2+H2O ![]() H++Cl-+HClO,见光2HClO=2HCl+O2↑,减小生成物浓度,促使平衡向正反应方向进行,即氯水颜色变浅,可以用勒夏特列原理解释,故D不符合题意;
H++Cl-+HClO,见光2HClO=2HCl+O2↑,减小生成物浓度,促使平衡向正反应方向进行,即氯水颜色变浅,可以用勒夏特列原理解释,故D不符合题意;
答案:C。

【题目】某小组同学探究物质的溶解度大小与沉淀转化方向之间的关系。
(查阅资料)
物质 | BaSO4 | BaCO3 | AgI | AgCl |
溶解度/g(20℃) | 2.4×10-4 | 1.4×10-3 | 3.0×10-7 | 1.5×10-4 |
(实验探究)
(一)探究BaCO3和BaSO4之间的转化,实验操作如下所示:
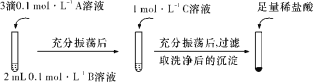
试剂A | 试剂B | 试剂C | 加入盐酸后的现象 | |
实验Ⅰ | ||||
实验Ⅱ | BaCl2 | |||
Na2CO3 | Na2SO4 | …… | ||
Na2SO4 | 有少量气泡产生,沉淀部分溶解 |
(1)实验Ⅰ说明BaCO3全部转化为BaSO4,依据的现象是加入稀盐酸后,__________。
(2)实验Ⅱ中加入稀盐酸后发生反应的离子方程式是_________。
(3)实验Ⅱ说明沉淀发生了部分转化,结合BaSO4的沉淀溶解平衡解释原因:___________。
(二)探究AgCl和AgI之间的转化。
(4)实验Ⅲ:证明AgCl转化为AgI。
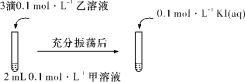
甲溶液可以是______(填字母代号)。
a AgNO3溶液 b NaCl溶液 c KI溶液
(5)实验Ⅳ:在试管中进行溶液间反应时,同学们无法观察到AgI转化为AgCl,于是又设计了如下实验(电压表读数:a>c>b>0)。
装置 | 步骤 | 电压表读数 |
| ||
ⅰ.按图连接装置并加入试剂,闭合K | a | |
ⅱ.向B中滴入AgNO3(aq),至沉淀完全 | b | |
ⅲ.再向B中投入一定量NaCl(s) | c | |
ⅳ.重复ⅰ,再向B中加入与ⅲ等量的NaCl(s) | a |
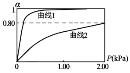
注:其他条件不变时,参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,原电池的电压越大;离子的氧化性(或还原性)强弱与其浓度有关。
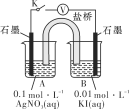
①查阅有关资料可知,Ag+可氧化I-,但AgNO3溶液与KI溶液混合总是得到AgI沉淀,原因是氧化还原反应速率__________(填“大于”或“小于”)沉淀反应速率。设计(-)石墨(s)[I-(aq)//Ag+(aq)]石墨(s)(+)原电池(使用盐桥阻断Ag+与I-的相互接触)如上图所示,则该原电池总反应的离子方程式为________。
②结合信息,解释实验Ⅳ中b<a的原因:__________。
③实验Ⅳ的现象能说明AgI转化为
(实验结论)溶解度小的沉淀容易转化为溶解度更小的沉淀,反之则不易;溶解度差别越大,由溶解度小的沉淀转化溶解度较大的沉淀越难实现。
【题目】苯甲醛是一种重要的化工原料,某小组同学利用如图所示实验装置(夹持装置已略去)制备苯甲醛。
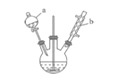
已知有机物的相关数据如下表所示:
有机物 | 沸点℃ | 密度为g/cm3 | 相对分子质量 | 溶解性 |
苯甲醛 | 178.1 | 1.04 | 106 | 微溶于水,易溶于乙醇、醚和卤代烃 |
苯甲醇 | 205.7 | 1.04 | 108 | 微溶于水,易溶于乙醇、醚和卤代烃 |
二氯甲烷 | 39.8 | 1.33 | 难溶于水,易溶于有机溶剂 |
实验步骤:
①向容积为500mL的三颈烧瓶加入90.0mL质量分数为5%的次氯酸钠溶液(稍过量),调节溶液的pH为9-10后,加入3.0mL苯甲醇、75.0mL二氯甲烷,不断搅拌。
②充分反应后,用二氯甲烷萃取水相3次,并将有机相合并。
③向所得有机相中加入无水硫酸镁,过滤,得到有机混合物。
④蒸馏有机混合物,得到2.08g苯甲醛产品。
请回答下列问题:
(1)仪器b的名称为______,搅拌器的作用是______。
(2)苯甲醇与NaClO反应的化学方程式为_______。
(3)步骤①中,投料时,次氯酸钠不能过量太多,原因是____;步骤③中加入无水硫酸镁,若省略该操作, 可能造成的后果是______。
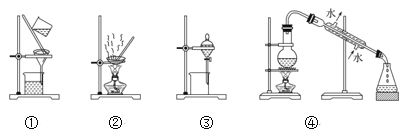
(4)步骤②中,应选用的实验装置是___(填序号),该操作中分离出有机相的具体操作方法是___。
(5)步骤④中,蒸馏温度应控制在_______左右。
(6)本实验中,苯甲醛的产率为________(保留到小数点后一位)。