题目内容
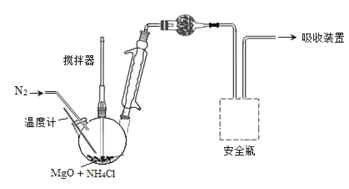
【题目】苯甲醛是一种重要的化工原料,某小组同学利用如图所示实验装置(夹持装置已略去)制备苯甲醛。

已知有机物的相关数据如下表所示:
有机物 | 沸点℃ | 密度为g/cm3 | 相对分子质量 | 溶解性 |
苯甲醛 | 178.1 | 1.04 | 106 | 微溶于水,易溶于乙醇、醚和卤代烃 |
苯甲醇 | 205.7 | 1.04 | 108 | 微溶于水,易溶于乙醇、醚和卤代烃 |
二氯甲烷 | 39.8 | 1.33 | 难溶于水,易溶于有机溶剂 |
实验步骤:
①向容积为500mL的三颈烧瓶加入90.0mL质量分数为5%的次氯酸钠溶液(稍过量),调节溶液的pH为9-10后,加入3.0mL苯甲醇、75.0mL二氯甲烷,不断搅拌。
②充分反应后,用二氯甲烷萃取水相3次,并将有机相合并。
③向所得有机相中加入无水硫酸镁,过滤,得到有机混合物。
④蒸馏有机混合物,得到2.08g苯甲醛产品。
请回答下列问题:
(1)仪器b的名称为______,搅拌器的作用是______。
(2)苯甲醇与NaClO反应的化学方程式为_______。
(3)步骤①中,投料时,次氯酸钠不能过量太多,原因是____;步骤③中加入无水硫酸镁,若省略该操作, 可能造成的后果是______。
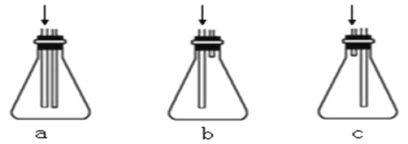
(4)步骤②中,应选用的实验装置是___(填序号),该操作中分离出有机相的具体操作方法是___。

(5)步骤④中,蒸馏温度应控制在_______左右。
(6)本实验中,苯甲醛的产率为________(保留到小数点后一位)。
【答案】球形冷凝管 使物质充分混合 ![]() + NaClO→
+ NaClO→![]() + NaCl+H2O 防止苯甲醛被氧化为苯甲酸,使产品的纯度降低 产品中混有水,纯度降低 ③ 打开分液漏斗颈部的玻璃塞(或使玻璃塞上的凹槽对准分液漏斗上的小孔),再打开分液漏斗下面的活塞,使下层液体慢慢沿烧杯壁流下,当有机层恰好全部放出时,迅速关闭活塞 178.1℃ 67.9%
+ NaCl+H2O 防止苯甲醛被氧化为苯甲酸,使产品的纯度降低 产品中混有水,纯度降低 ③ 打开分液漏斗颈部的玻璃塞(或使玻璃塞上的凹槽对准分液漏斗上的小孔),再打开分液漏斗下面的活塞,使下层液体慢慢沿烧杯壁流下,当有机层恰好全部放出时,迅速关闭活塞 178.1℃ 67.9%
【解析】
(1)根据图示结合常见的仪器的形状解答;搅拌器可以使物质充分混合,反应更充分;
(2)根据实验目的,苯甲醇与NaClO反应生成苯甲醛;
(3)次氯酸钠具有强氧化性,除了能够氧化苯甲醇,也能将苯甲醛氧化;步骤③中加入无水硫酸镁的目的是除去少量的水;
(4)步骤②中萃取后要进行分液,结合实验的基本操作分析解答;
(5)步骤④是将苯甲醛蒸馏出来;
(6) 首先计算3.0mL苯甲醇的物质的量,再根据反应的方程式计算理论上生成苯甲醛的质量,最后计算苯甲醛的产率。
(1)根据图示,仪器b为球形冷凝管,搅拌器可以使物质充分混合,反应更充分,故答案为:球形冷凝管;使物质充分混合;
(2)根据题意,苯甲醇与NaClO反应,苯甲醇被氧化生成苯甲醛,次氯酸钠本身被还原为氯化钠,反应的化学方程式为![]() + NaClO→
+ NaClO→![]() + NaCl+H2O,故答案为:
+ NaCl+H2O,故答案为:![]() + NaClO→
+ NaClO→![]() + NaCl+H2O;
+ NaCl+H2O;
(3)次氯酸钠具有强氧化性,除了能够氧化苯甲醇,也能将苯甲醛氧化,因此步骤①中,投料时,次氯酸钠不能过量太多;步骤③中加入无水硫酸镁的目的是除去少量的水,提高产品的纯度,若省略该操作,产品中混有水,纯度降低,故答案为:防止苯甲醛被氧化为苯甲酸,使产品的纯度降低;产品中混有水,纯度降低;
(4)步骤②中,充分反应后,用二氯甲烷萃取水相3次,萃取应该选用分液漏斗进行分液,应选用的实验装置是③,分液中分离出有机相的具体操作方法为打开分液漏斗颈部的玻璃塞(或使玻璃塞上的凹槽对准分液漏斗上的小孔),再打开分液漏斗下面的活塞,使下层液体慢慢沿烧杯壁流下,当有机层恰好全部放出时,迅速关闭活塞,故答案为:③;打开分液漏斗颈部的玻璃塞(或使玻璃塞上的凹槽对准分液漏斗上的小孔),再打开分液漏斗下面的活塞,使下层液体慢慢沿烧杯壁流下,当有机层恰好全部放出时,迅速关闭活塞;
(5)根据相关有机物的数据可知,步骤④是将苯甲醛蒸馏出来,蒸馏温度应控制在178.1℃左右,故答案为:178.1℃;
(6)根据![]() + NaClO→
+ NaClO→![]() + NaCl+H2O可知,1mol苯甲醇理论上生成1mol苯甲醛,则3.0mL苯甲醇的质量为1.04 g/cm3×3.0cm3=3.12g,物质的量为
+ NaCl+H2O可知,1mol苯甲醇理论上生成1mol苯甲醛,则3.0mL苯甲醇的质量为1.04 g/cm3×3.0cm3=3.12g,物质的量为![]() ,则理论上生成苯甲醛的质量为
,则理论上生成苯甲醛的质量为![]() ×106g/mol=3.06g,苯甲醛的产率=
×106g/mol=3.06g,苯甲醛的产率=![]() ×100%=67.9%,故答案为:67.9%。
×100%=67.9%,故答案为:67.9%。

 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案