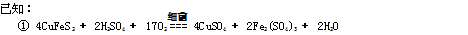题目内容
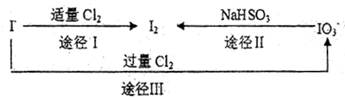
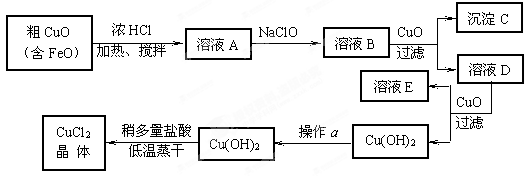
海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:

请填写下列空白:
(1)步骤⑤的操作名称是 用到的主要仪器是:
(2)步骤③的实验操作名称是 ;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是 。

请填写下列空白:
(1)步骤⑤的操作名称是 用到的主要仪器是:
(2)步骤③的实验操作名称是 ;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是 。
(1)萃取 分液漏斗 (2)过滤,蒸馏
考查碘的提取、物质的分离
海带灼烧后,将灰浸泡可得到悬浊液,通过过滤可滤除不溶物,得到含有碘离子的溶液;用氧化剂将碘离子氧化后,用萃取剂来提取出单质碘,再蒸馏即可得到碘单质
(1)萃取的主要仪器是分液漏斗 (2)过滤、蒸馏
海带灼烧后,将灰浸泡可得到悬浊液,通过过滤可滤除不溶物,得到含有碘离子的溶液;用氧化剂将碘离子氧化后,用萃取剂来提取出单质碘,再蒸馏即可得到碘单质
(1)萃取的主要仪器是分液漏斗 (2)过滤、蒸馏

练习册系列答案
相关题目