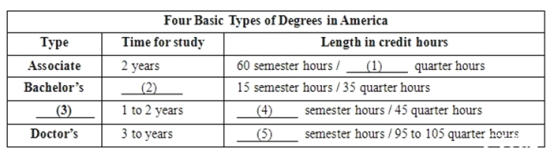
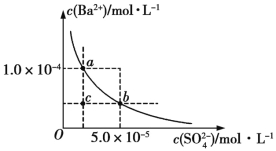
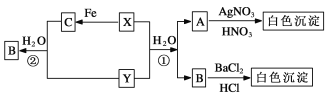
��Ŀ����
����Ŀ����������ѧ̼��������ʱ���鵽���������ϣ�
��CO2+Na2CO3+H2O===2NaHCO3��CO2ͨ�뱥��̼������Һ�������ɫ������CO2�����ڱ���̼��������Һ��
��̼���ơ�̼�������ڲ�ͬ�¶��µ��ܽ�������
0 �� | 10 �� | 20 �� | 30 �� | |
Na2CO3 | 7.1 | 12.2 | 21.8 | 39.7 |
NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 |
������ʵ��1����֤CO2ͨ�뱥��̼������Һ�������ɫ����
������̼������Һ��ȡ100 g 20 ����ˮ������35 g̼���ƹ��壬������ã�ȡ�ϲ���Һ��
������װ��һ����ʵ�飬����5���������Ƶõ�̼������Һ��ͨ��CO2��
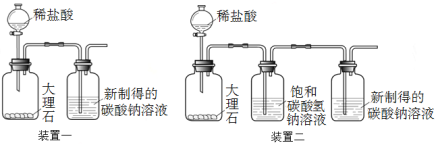
���������⡿ʵ���У�ʼ��û�п�����������ԭ����ʲô�أ���������������ʵ��̽����
������ʵ��2��
ʵ����� | ʵ������ |
��ȡ100 g 20 ����ˮ������35 g̼���ƹ��壬������ã�ȡ�ϲ���Һ ������װ�ö�����ʵ�飬����5���������Ƶõ�̼������Һ��ͨ��CO2 | û�г��ְ�ɫ���� |
(1)��0 ��~30 ����Na2CO3��NaHCO3���ܽ�����¶ȱ仯Ӱ��ϴ���� ��
(2)����ʯ��ϡ���ᷴӦ�Ļ�ѧ����ʽΪ ��
(3)װ�ö��б���̼��������Һ�������� ��
������ʵ��3��
ʵ����� | ʵ������ |
��ȡ100 g�ȿ�ˮ������35 g̼���ƹ��壬��ȫ�ܽ⣬�ٽ�����20 ����ȡ�ϲ���Һ ������װ��һ��װ�ö��ֱ����ʵ�飬����3���������Ƶõ�̼������Һ��ͨ��CO2 | װ��һ��װ�ö��е�̼������Һ�о����ְ�ɫ���� |
(4)�����������ʵ����û�п������������ԭ���� ��
(5)CO2ͨ�뱥��̼������Һ�������ɫ������ԭ���� ��
(6)��������������Ϣ��д��һ���ܹ�����̼���ƺ�̼�����ƹ����ʵ�鷽�� ��
���𰸡�(1) Na2CO3
(2)CaCO3 +2HCl===CaCl2+H2O+CO2��
(3)�ų�HCl�ĸ���
(4)���Ƶ�̼������Һû�дﵽ����
(5)̼�������ܽ��С��̼���ƣ�ˮ���٣����ɵ�̼�����Ƶ��������ڷ�Ӧ��̼����
(6)����һ��ȡ����һ�ֹ���12 g������100 g�ȿ�ˮ������ܽ������20 �������й���������Ϊ̼�����ƣ�����Ϊ̼����
��������ȡ����һ�ֹ���12 g������100 g 20 ����ˮ������ܽ�����а�ɫ����ʣ�࣬Ϊ̼�����ƣ�����Ϊ̼����
��������(1)��0����30����Na2CO3��NaHCO3���ܽ�����¶ȱ仯Ӱ��ϴ����Na2CO3��
(2)����ʯ��ϡ���ᷴӦ�Ļ�ѧ����ʽΪCaCO3+2HCl===CaCl2+H2O+CO2����
(3)���ɵ�CO2�л����Ȼ������壬���װ�ö��б���̼��������Һ�������������Ȼ������壬�Ӷ��ų��Ȼ��������ʵ��ĸ��š�
(4)�����������ʵ����û�п������������ԭ�������Ƶ�̼������Һû�дﵽ���͡�
(5)����̼�������ܽ��С��̼���ƣ����ŷ�Ӧ�Ľ��У�ˮ��������С�����ɵ�̼�����Ƶ��������ڷ�Ӧ��̼���ƣ�����CO2ͨ�뱥��̼������Һ�������ɫ����̼�����ơ�
(6)���ݱ������ʵ��ܽ�����ݿ�֪����̼���ƺ�̼�����ƹ����ʵ�鷽�������֣�
����һ��ȡ����һ�ֹ���12 g������100 g�ȿ�ˮ������ܽ������20 �������й���������Ϊ̼�����ƣ�����Ϊ̼���ƣ���������ȡ����һ�ֹ���12 g������100 g 20 ����ˮ������ܽ�����а�ɫ����ʣ�࣬Ϊ̼�����ƣ�����Ϊ̼���ơ�