题目内容
【题目】某化学课外小组欲制取纯净的Na2CO3溶液并讨论实验过程中的相关问题。可供选择的试剂有:
A.大理石 B.盐酸
C.氢氧化钠溶液 D.澄清石灰水
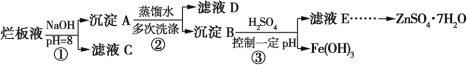
三名同学设计的制备实验方案的反应流程分别如下:
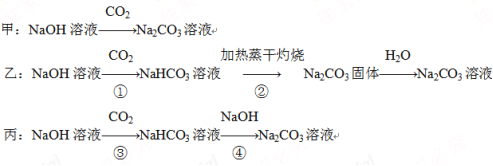
请回答下列问题:
(1)请指出甲、乙两方案的主要缺点:
甲方案:______________________________________________________。
乙方案:______________________________________________________。
(2)假设反应③所得的NaHCO3溶液中含有Na2CO3,现要用A~D四种试剂证明Na2CO3的存在,你所选择的试剂有________________。
【答案】(1)由于难以控制CO2的量,故很难得到纯净的Na2CO3 原料利用率低,程序复杂 (2)BD
【解析】(1)NaOH与CO2反应时两者量不同,产物不同,2OH+CO2===![]() +H2O,OH+CO2===
+H2O,OH+CO2===![]() ,甲不能控制通入CO2的物质的量,也就不能控制产物为纯净的Na2CO3。乙的操作程序复杂。丙应将NaOH溶液分成两等份,一份通入足量CO2,加热赶出其中溶解的CO2,再将另一份NaOH溶液与NaHCO3溶液混合即可得到纯净的Na2CO3溶液。
,甲不能控制通入CO2的物质的量,也就不能控制产物为纯净的Na2CO3。乙的操作程序复杂。丙应将NaOH溶液分成两等份,一份通入足量CO2,加热赶出其中溶解的CO2,再将另一份NaOH溶液与NaHCO3溶液混合即可得到纯净的Na2CO3溶液。
(2)检验NaHCO3溶液中含有Na2CO3,应向溶液中加入BaCl2或CaCl2,所以应选盐酸和澄清石灰水,二者生成CaCl2再检验。

练习册系列答案
 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目