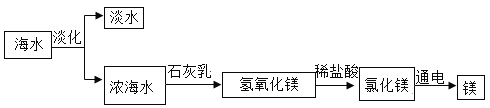
【题目】实验室中有一瓶长期使用的氢氧化钠固体样品,某兴趣小组的同学对该样品的成分及含量进行探究
[发现问题]该样品中含有哪些物质?
[查阅资料]①NaOH在空气中不会转化成NaHCO3②BaCl2溶液呈中性,Ba(OH)2是可溶性碱③CO2在饱和的NaHCO3溶液中几乎不溶解
[提出猜想]猜想Ⅰ:NaOH
猜想Ⅱ:Na2CO3
猜想Ⅲ:NaOH和Na2CO3
[设计实验]
实验操作 | 实验现象 |
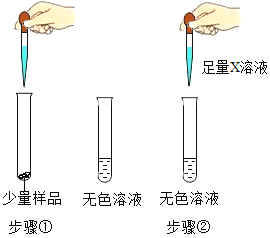
| 步骤(1):样品全部溶解 步骤(2):观察到现象A |
[收集证据](1)若现象A是有气泡产生,则x为_______溶液 (填化学式),则_______(填“猜想Ⅰ”、“猜想Ⅱ” 或“猜想Ⅲ”)不成立。
(2)若X溶液为Ba(OH)2溶液,现象A是有白色沉淀生成,则产生沉淀的化学方程式是______。取反应后的上层清液,测定其pH>7,则证明猜想Ⅲ成立,这个结论是否正确_______(填“是”或“否”)。
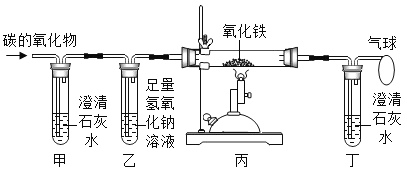
[定量分析]确定部分变质样品中Na2CO3的质量分数,兴趣小组的同学用如图所示装置进行实验。
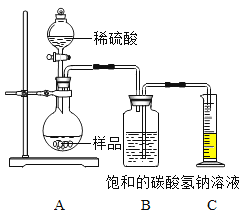
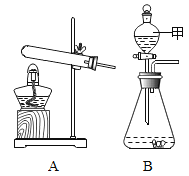
步骤如下:①按图连接好装置,井检查气密性:②准确称取该样品1.0g放入烧瓶内;③打开活塞,滴加30.0%的稀硫酸至过量,关闭活塞;④反应结束后,量筒内液体的读数为55.0mL.(已知:室温条件下,CO2的密度为1.6g﹒L-1 )
(1)B装置集气瓶内原有的空气对实验结果_______(填 “有”或“没有”)影响。B中饱和NaHCO3溶液如果用水代替,则所测CO2体积______(填 “偏大”、“偏小”或“不变”)。
(2)通过计算,便可测得该样品中Na2CO3的质量分数。______
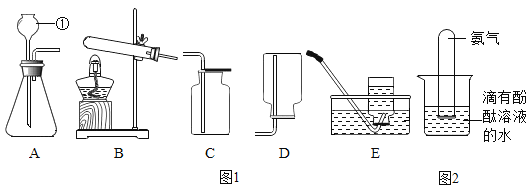
【题目】根据下列实验装置图,回答问题
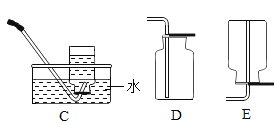
发生装置 | 收集装置 | 洗气装置 |
|
|
|
(1)说出仪器甲的名称________。
(2)实验室用过氧化氢和二氧化锰制取氧气的化学方程式为________。可选择的发生装置为________(填字母)。
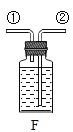
(3)实验室用石灰石和稀盐酸反应制取二氧化碳的化学方程式为________。该反应生成的二氧化碳气体中常混有少量氯化氢气体,可通过盛有饱和碳酸氢钠溶液的F装置除去氯化氢气体,则该混合气体应从F装置的_______(填“①”或“②”)口通入。
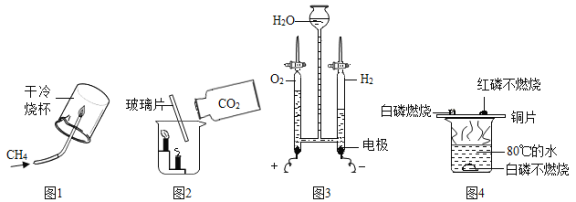
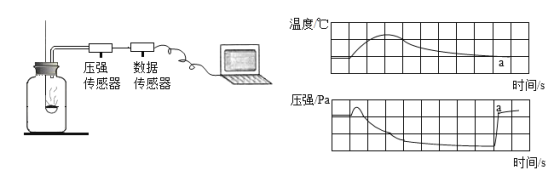
【题目】理科实验操作考试中有关于探究金属的某些物理性质和化学性质的试题,用坩埚钳夹取打磨过的铜片在酒精灯上加热,发现铜片表面变黑,为了探究黑色物质的成分。
(查阅资料)(1)铜的氧化物主要有两种:CuO(黑色);Cu2O(红色)
(2)酒精在不完全燃烧时会产生炭黑
(3)炭黑不与稀硫酸反应,也不溶于稀硫酸;氧化铜可与稀硫酸反应而溶解
(提出假设)猜想1:黑色物质为_____________。
猜想2:黑色物质为炭黑。
猜想3:黑色物质为_____________。
(设计方案)
操作步骤 | 实验中可能出现的现象 | 实验结论 |
取少量黑色固体于试管中,加入 足量___________(填物质名称) | ①_______ | 猜想1成立 |
② 黑色固体没有减少,溶液颜色不变 | 猜想2成立 | |
③_______ | 猜想3成立 |
(得出结论)通过实验现象,得出猜想3成立,此黑色固体为混合物。请写出实验中发生的化学方程式____________。
【题目】某化学学习小组在老师的指导下,对白色粉笔的成分进行探究。
(提出问题)白色粉笔的主要成分是什么呢?老师提示是一种常见的钙盐与少量性质稳定的粘合剂制成的。
(猜想与假设)同学分别做出如下猜想:
A:碳酸钙 B:氢氧化钙 C:硫酸钙 D:氯化钙 E:硝酸钙
同学们根据老师提示并讨论,立即否定了B的猜想,你认为理由是______。
(查阅资料)
(1)硫酸钙是自然界中石膏矿的主要成分,为白色固体,微溶于水。
(2)室温下几种物质的溶解度
物质 | 碳酸钙 | 氯化钙 | 硫酸钙 | 硝酸钙 |
溶解度/g | 0.0013 | 74.5 | 0.3 | 138 |
(进行实验)
实验操作 | 现象 | 结论 | |
① | 取少量白色粉笔研碎于试管中,加入 ______ | 无现象 | A不成立 |
② | 取少量白色粉笔研碎于烧杯中,加入少量水,搅拌 | 固体没有明显减少 | ______ 不成立 |
③ | 将②进行 ______ 操作,得到清液A和固体,向清液中加入 ______ 溶液,再加入足量稀盐酸 | 产生白色沉淀,沉淀不消失 | C成立 |
请写出③中发生反应的化学方程式______。
注意:若答对以下问题可奖励4分,化学试卷总分不超过60分。
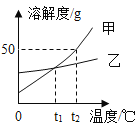
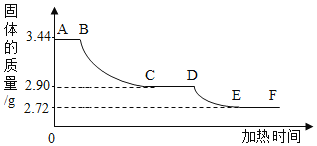
(拓展延伸)为了测定生石膏的组成(CaSO4xH2O),即测定x的值,做了如下实验:将含结晶水的硫酸钙放在坩埚中加热,加热前和加热后都进行称量。随着实验次数的增加,加热的时间不断延长,他们在实验中将数据整理如下,并利用数据绘制的图象如图所示。
查阅资料:含结晶水的硫酸钙有两种组成形式,在加热过程中,分步失去结晶水,最终得到硫酸钙固体。
实验顺序 (按序延长加热时间) | 固体质量/g | |
加热前 | 加热后 | |
1 | 3.44 | 3.26 |
2 | 3.44 | 3.12 |
3 | 3.44 | 2.90 |
4 | 3.44 | 2.90 |
5 | 3.44 | 2.80 |
6 | 3.44 | 2.78 |
7 | 3.44 | 2.72 |
8 | 3.44 | 2.72 |
(1)AB段固体质量不变的原因______。
(2)利用实验数据,计算x=______。
(3)图中CD段固体物质的化学式______。