题目内容
【题目】理科实验操作考试中有关于探究金属的某些物理性质和化学性质的试题,用坩埚钳夹取打磨过的铜片在酒精灯上加热,发现铜片表面变黑,为了探究黑色物质的成分。
(查阅资料)(1)铜的氧化物主要有两种:CuO(黑色);Cu2O(红色)
(2)酒精在不完全燃烧时会产生炭黑
(3)炭黑不与稀硫酸反应,也不溶于稀硫酸;氧化铜可与稀硫酸反应而溶解
(提出假设)猜想1:黑色物质为_____________。
猜想2:黑色物质为炭黑。
猜想3:黑色物质为_____________。
(设计方案)
操作步骤 | 实验中可能出现的现象 | 实验结论 |
取少量黑色固体于试管中,加入 足量___________(填物质名称) | ①_______ | 猜想1成立 |
② 黑色固体没有减少,溶液颜色不变 | 猜想2成立 | |
③_______ | 猜想3成立 |
(得出结论)通过实验现象,得出猜想3成立,此黑色固体为混合物。请写出实验中发生的化学方程式____________。
【答案】氧化铜 炭黑和氧化铜的混合物 稀硫酸 黑色固体消失,溶液变蓝 溶液变蓝,固体有剩余 CuO+H2SO4=CuSO4+H2O
【解析】
打磨过的铜片在酒精灯上加热,发现铜片表面变黑,铜在加热条件下和氧气反应生成黑色物质,炭黑不与稀硫酸反应,也不溶于稀硫酸,氧化铜与稀硫酸反应生成硫酸铜和水。
[提出假设]猜想1:黑色物质为氧化铜。
猜想2:黑色物质为炭黑。
猜想3:黑色物质为炭黑和氧化铜的混合物。
[设计方案]
操作步骤 | 实验中可能出现的现象 | 实验结论 |
取少量黑色固体于试管中,加入 足量稀硫酸 | ①黑色固体消失,溶液变蓝 | 猜想1成立 |
②黑色固体没有减少,溶液颜色不变 | 猜想2成立 | |
③溶液变蓝,固体有剩余 | 猜想3成立 |
[得出结论]
炭黑不与稀硫酸反应,也不溶于稀硫酸,氧化铜与稀硫酸反应生成硫酸铜和水,通过实验现象,得出猜想3成立,此黑色固体为混合物。实验中发生的化学方程式![]() 。
。

【题目】生理盐水是0.9%的氯化钠水溶液,因为它的渗透压值和正常人的血浆、组织液都是大致一样的,所以可以用作补液以及其他医疗用途。已知氯化钠在不同温度时的溶解度如下表所示:
温度/℃ | 0 | 10 | 20 | 40 | 60 | 80 |
溶解度/g | 35.7 | 35.8 | 36.0 | 36.6 | 37.3 | 38.4 |
下列说法中不正确的是( )
A. 氯化钠的溶解度随着温度的升高而增大
B. 20℃时的生理盐水是氯化钠的不饱和溶液
C. 将80℃时的氯化钠的饱和溶液冷却至20℃,有结晶现象
D. 40℃时,100g氯化钠的饱和溶液中氯化钠的质量为36.6g
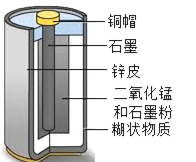
【题目】我校兴趣小组对废旧的干电池进行探究,同学们首先将干电池剖开发现有一层白色糊状物质,并闻到一股氨味。
(提出问题)白色糊状物的成分是什么?
(提供资料)
① 干电池的内部结构见如图,白色糊状物质A中除了含有淀粉,还含有一种盐,且该盐中阴离子是SO42-、CO32-、Cl-中的一种。
② 碘溶液能使淀粉变蓝。
③ 氨气可以使湿润的红色石蕊试纸变蓝。
(进行猜想)A中含有淀粉,A中的盐可能是铵盐。
(实验一)取少量A于试管中,滴加少量碘溶液,观察到_______________,证明A中含有淀粉。
(实验二)取少量A于研钵中,加入_____________固体,混合、研磨,产生刺激性气味的气体,该气体能使湿润的红色石蕊试纸变蓝,证明A中含有铵根离子。
(实验三)为了验证其阴离子的存在情况,兴趣小组再次设计如下实验,请你完成以下实验报告。
实验操作 | 实验现象 | 实验结论 |
(1)取糊状物少量,加足量的水,搅拌后过滤。取少量滤液于试管中,滴加氯化钡溶液。 | 无现象 | ________________ |
(2)另取第(1)步所得滤液少量,滴加少量_____________溶液 | 产生白色沉淀 | 存在的离子是Cl- |
(得出结论)上述实验证明,电池内白色糊状物含有淀粉和氯化铵两种物质。
(反馈交流)兴趣小组指导老师指出实验三的方案设计存在错误,请你说明错误的原因并将其改正:___________________________。
(知识应用)回收废旧干电池不仅可以减少环境污染,还能变废为宝。根据上述探究过程,请简要说明干电池中的白色糊状物的回收价值有:__________________________________。