【题目】现实验室中有一包由碳酸钠和氧化钙组成的白色粉末,下面是某化学兴趣小组的同学进行的探究过程,请你按要求帮助完成探究活动。
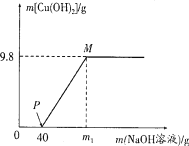
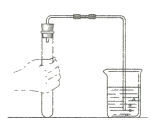
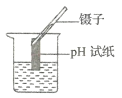
同学们将部分白色固体放于烧杯中加入少量的水,发现烧杯外壁有热感,加水放热的反应的化学方程式是_______________。继续加入足量的水并过滤,用pH试纸测定滤液的pH, pH_______________7 (选填“>、=、<”)。滤液呈碱性。
(提出问题)滤液中含有那些碱性物质?
(提出猜想)
猜想①: NaOH
猜想②: NaOH 和Na2CO3
猜想③: NaOH和Ca(OH)2
猜想④: NaOH、Ca(OH)2 和Na2CO3
[查阅资料] Na2CO3溶液呈碱性
(实验探究)
(1)甲同学认为猜想④不合理,原因是__________________(用化学方程式表示)。
(2)乙同学进行下列实验,请你填写表中空白处。
实验操作步骤 | 实验现象 | 结论 |
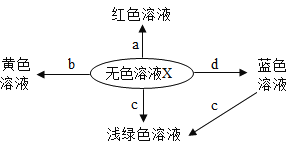
I.取用少量滤液于试管中,通入CO2 | 没有明显变化 | 滤液不含_________。 |
Ⅱ.取用少量滤液于试管中,滴加过量CaCl2溶液,后滴入无色酚酞试液 | ____________ | 滤液含有Na2CO3;反应的化学方程式是_____________。 |
_____________ | 滤液含有NaOH。 |
(获得结论)猜想②成立
(反思拓展)
实验操作步骤Ⅱ中加入过量CaCl2溶液的目的是__________________________。