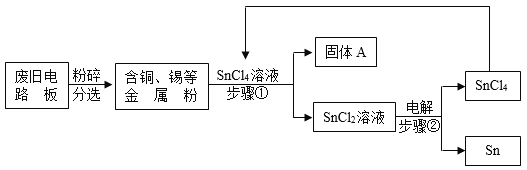
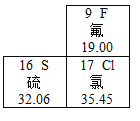
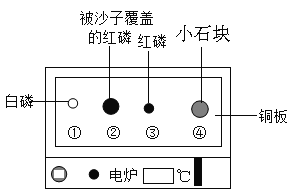
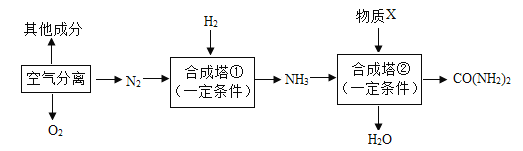
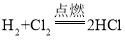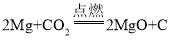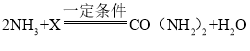【题目】某同学要探究燃烧的条件和空气中氧气的含量,进行了如下实验.
【实验一】(已知:白磷的着火点为40℃)
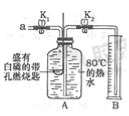
实验装置 | 实验步骤及现象 |
| 步骤Ⅰ.检验装置的气密性,气密性良好. 步骤Ⅱ.将盛有白磷的带孔燃烧匙伸入A瓶中,白磷不燃烧. 步骤Ⅲ.向A瓶中加满80℃热水,塞紧瓶塞,白磷不燃烧. 步骤Ⅳ.打开K1、K2,从a口向瓶中鼓入空气,待瓶中的液面低于燃烧匙底部时,关闭K1、K2.此时进入量筒B中水的体积为200mL,观察到A瓶中的白磷燃烧. |
(1)对比步骤Ⅱ和Ⅳ的现象可知,可燃物燃烧的条件之一是
(2)待装置冷却一段时间后,打开K2,如果观察到 ,说明空气中氧气的体积约占![]() .若实验测得空气中氧气的体积分数小于
.若实验测得空气中氧气的体积分数小于![]() ,原因可能是 (答一条即可).
,原因可能是 (答一条即可).
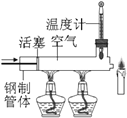
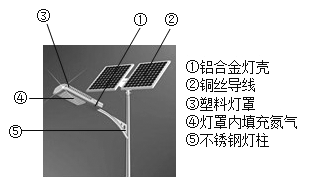
【实验二】用如图所示装置,利用铁生锈的原理也可以比较准确地测出空气中氧气的含量.若将此装置中的细铁丝换成足量的细铜丝进行实验,能否比较准确地测出空气中氧气的含量,并说明理由 .【已知:铜能与空气中氧气、水、二氧化碳反应生成铜绿.化学方程式:2Cu+O2+H2O+CO2═Cu(OH)2CO3】
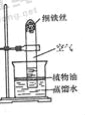
【题目】在一节实验课上,某兴趣小组对实验室制取二氧化碳展开了探究。
(1)按下表进行实验,取等质量的大理石加入足量酸中(杂质不与酸反应),产生的CO2体积随时间变化的曲线如图所示:
实验编号 | 药品 |
① | 块状大理石、10%稀硫酸 |
② | 块状大理石、7%稀盐酸 |
③ | 大理石粉末、7%稀盐酸 |
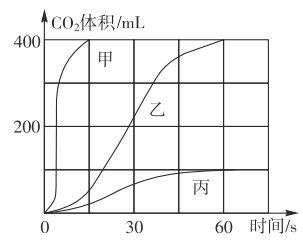
图中丙对应实验______(填实验编号)。对比甲和乙可以看出,影响化学反应快慢的因素之一是______。确定用乙对应的药品制取二氧化碳,反应的化学方程式为______。
(2)用乙对应的药品制取二氧化碳,当观察不到气泡产生时发现固体仍有剩余,小明对此展开探究(杂质不溶于水且不与酸反应)。
(提出问题)不再产生气泡的原因是什么?
(查阅资料)紫色石蕊是一种酸碱指示剂,在酸性溶液中会变成红色,在中性溶液中不变色;氯化钙溶液呈中性。
(作出猜想)猜想一:反应后溶液中无盐酸;
猜想二:剩余固体中无碳酸钙。
(实验探究一)反应后溶液中是否有盐酸?
①小丽取少量反应后的溶液,滴加紫色石蕊,观察到______,说明反应后溶液显______性,由此得出猜想一不成立。
②小明认为小丽的实验不严谨,还应考虑生成物对溶液酸碱性的影响,于是补充了如下两个实验:
实验A:配制______(填物质名称或化学式)溶液,并滴加紫色石蕊溶液,溶液不变色。实验B:在试管中加入适量水和紫色石蕊溶液,持续通入CO2,溶液变为______色。
③小华认为小明的实验也不够严谨,并再次改进实验,最终得出正确的结论:反应后的溶液中有盐酸,猜想一不成立。
(注意:若答对以下小题奖励4分,化学试卷总分不超过60分。)
(实验探究二)请设计实验,探究反应后的剩余固体中是否有碳酸钙?
实验步骤 | 实验现象 | 实验结论 |
_____ | ______ | ______ |