题目内容
【题目】如图是实验室制取气体的常用装置,请回答下列问题。
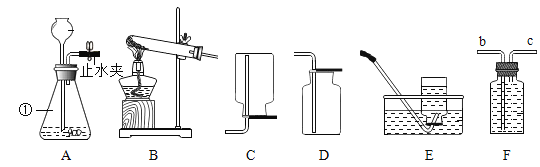
(1)写出图中标号仪器①的名称:_______。
(2)检查装置A气密性的方法是:夹紧止水夹,若________,则气密性良好。
(3)用锌粒和稀硫酸制取氢气,选择的发生装置为_______(填字母),反应的化学方程式为_______。用装置C而不用装置D收集氢气,原因是_______。
(4)用装置F和量筒收集并测量氢气的体积,在F中气体应从导管_______(填“b”或“c”)端通入。
【答案】锥形瓶 向长颈漏斗中加水,若一段时间内水柱液面不下降 A ![]() 氢气的密度比空气小 c
氢气的密度比空气小 c
【解析】
(1)仪器①为锥形瓶;
(2)检查装置A气密性的方法是:夹紧止水夹,向长颈漏斗中加水,若一段时间内水柱液面不下降,则气密性良好;
(3)用锌粒和稀硫酸制取氢气,属于固液不加热型反应,故发生装置应选A;
锌与稀硫酸反应生成硫酸锌和氢气,其化学反应方程式为:![]() ;
;
氢气的密度比空气小,应用向下排空气法收集,故应用装置C而不用装置D 收集氢气;
(4)氢气的密度比水小,因此用装置F和量筒收集并测量氢气的体积,在F中气体应从导管c端通入。

【题目】实验室有一瓶标签受到腐蚀(如图所示)的无色溶液,老师叫各小组开展探究。

(提出问题)
这瓶无色溶液究竟是什么物质的溶液?
(猜想与假设)
经了解得知,这瓶无色溶液原来是放在存放盐溶液的柜子里。由此猜测:可能是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中某一种。
(理论分析)
为了确定该溶液,他们首先进行了
(1)甲同学根据标签上的组成元素认为一定不可能是_____溶液。
(2)乙同学提出,碳酸氢钠、硝酸钠的溶液也不可能,他的依据是_____。
(设计实验)
为了确定该溶液究竟是剩余两种盐的哪一种溶液,他们设计了如下实验:
实验操作 | 实验现象 |
①取少量该无色溶液于试管中,慢慢滴加BaCl2溶液 ②静置后,倒出上层清液,向沉淀中滴加稀盐酸 | 产生白色沉淀 产生大量气泡,沉淀消失 |
(实验结论)
(3)该瓶无色溶液是_____。
(实验反思)
(4)丙同学认为原设计的实验还可简化,同样达到鉴别的目的。丙同学设计的实验如下(将实验操作及实验现象填入相应的空格中):
实验操作 | 实验现象 |
_____ | _____ |
(5)下列物质能与Na2CO3溶液反应产生与步骤①类似实验现象的是_____。
A Ba(OH)2 B CaCl2 C KNO3 D H2SO4
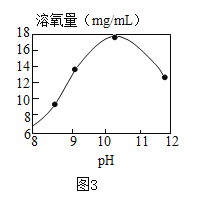
【题目】某研究性学习小组在进行“利用燃碳法测定空气中氧气的休积分数”的实验时(装置如图甲所示),发现一个现象:氢氧化钠溶液(易吸收二氧化碳而不吸收一 氧化碳) 吸收生成的二氧化碳后,进入集气瓶中水的体积分数仍然小于1/5。
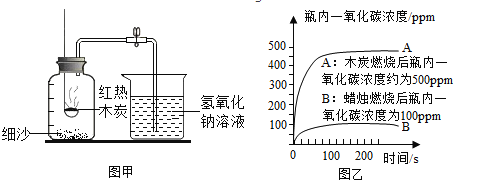
(1)教材中利用燃烧红磷法测定空气中氧气的体积分数,选择该药品的原因是:_________________、________________。
(2)[提出问题]测量不准确的原因是什么呢?
[猜想与假设]他们分别作出如下猜想:
甲同学:可能是木炭的量过少;
乙同学:可能是木炭足量,但其燃烧没有消耗完集气瓶中的氧气;
丙同学:可能是木炭燃烧生成了一氧化碳。
小组同学发现实验结束后,燃烧匙中还残留有黑色固体,因此他们都认为甲同学的猜想不合理。
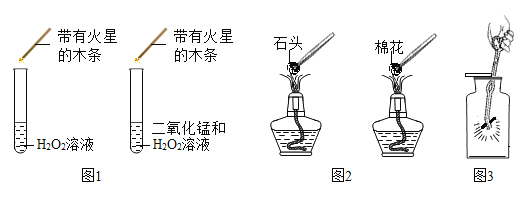
[查阅资料]木炭、棉花和蜡烛在密闭容器内燃烧停止后,残留氧气的体积分数分别高达 14. 0%、8. 0%和16. 0%。
乙同学根据如图所示装置设计了如下实验,请你填写下表:
实验步骤 | 实验现象 | 实验结论 |
将足量木炭点燃,迅速插入集气瓶中 | 木炭先继续燃烧,一段时间后熄灭 | 木炭燃烧没有消耗完集气瓶中的氧气 |
待集气瓶冷却后,将燃着的____________,(填“棉花”或“蜡烛”)再伸入该集气瓶中 | _______________。 |
[交流与反思]请写出木炭不完全燃烧的化学方程式:________________。
(3)木炭熄灭后,乙同学选择可燃物的依据是_____________________。
(4)丙同学使用一氧化碳浓度传感器测得木炭、蜡烛分别在密闭集气瓶里燃烧停止后瓶内一氧化碳的浓度变化曲线如乙图。根据此曲线图分析用上述装置不能准确测出氧气体积分数的原因___________________。
(5)在实际实验过程中,有部分燃碳法实验测定的空气中氧气的体积分数可以达到20%,推测造成这一现象的原因:__________________。