【题目】某化学兴趣小组针对教科书中两个实验进行再探究。
(探究一)空气中氧气含量测定的再认识
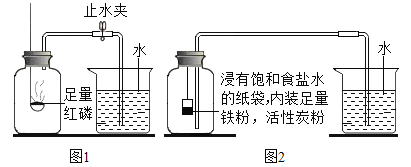
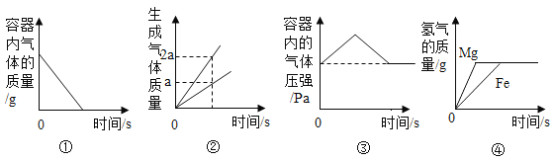
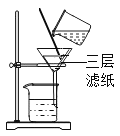
(1)测定装置如图1所示,红磷燃烧消耗氧气,使集气瓶内_____减小,烧杯中的水倒吸进入集气瓶。但该实验误差较大,测得空气中氧气含量明显低于![]() 。
。
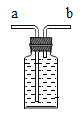
(实验改进)根据铁在空气中生锈的原理设计实验如图2所示,装置中饱和食盐水、活性炭能加快铁生锈的速率,测得数据如下表:
实验前 | 实验后 | |
烧杯中水的体积/mL | 烧杯中剩余水的体积/mL | 集气瓶(扣除内容物)和导管的容积/mL |
80.8 | 54.5 | 126.0 |
(2)根据上表信息,空气中氧气的体积分数为_____(只列式,不计算)。
(3)从实验原理角度分析,改进后的实验结果更准确的原因是_____(写一点)。
(探究二)铁在氧气中燃烧后所得固体物质成分的探究
(问题1)铁燃烧时溅落下来的黑色物质中是否含有铁?
(资料)① 自然界中铁的氧化物主要是Fe3O4(黑色)和Fe2O3(红棕色)两种;
② FeO(黑色)极易被氧化为Fe2O3;
③ 铁的氧化物均能与稀盐酸或稀硫酸反应生成铁的化合物溶液。
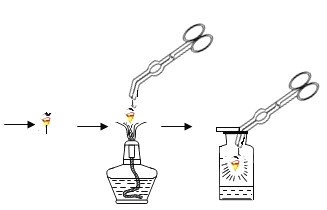
(实验)将冷却后的黑色物质碾碎,装入试管,加入_____溶液,观察到_____的现象,说明铁燃烧时溅落下来的黑色物质中含有铁。
(问题2)铁燃烧的产物为什么不是Fe2O3?
(资料)① Fe3O4和Fe2O3的分解温度、铁的熔点见表;
Fe3O4 | Fe2O3 | 铁 | |
分解温度/℃ | 1538 | 1400 | — |
熔点/℃ | — | — | 1535 |
② Fe2O3高温时分解成Fe3O4。
(证据推理)根据实验现象及表中信息可知,铁在氧气里燃烧时产生的高温应在_____之间,此时Fe2O3已分解。
(拓展延伸)(1)为了防止集气瓶炸裂,必须采取_____的措施。
(2)某食品密封包装盒的透明盖内放有黑色的FeO粉末,若颜色_____,说明包装盒漏气。
(3)Fe2O3高温时会分解成Fe3O4和一种气体,该反应的化学方程式为_____。