题目内容
【题目】燃烧是人类最早利用的化学反应之一。回答下列问题:

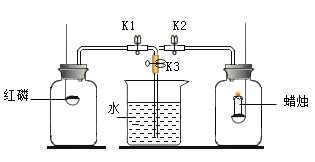
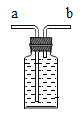
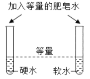
(1)① 甲实验中气球的作用是_____;通过观察_____(填“a”、“b”、“c”)处的现象,可得出燃烧需要氧气的结论。
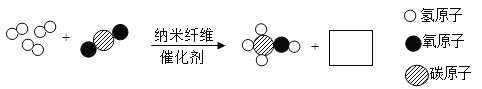
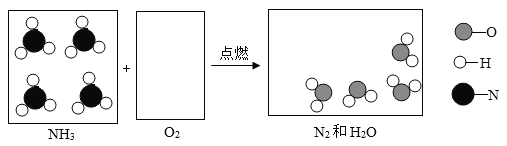
② 氨气在纯氧气中也能燃烧(4 NH3 + 3 O2 ![]() 2 N2 + 6 H2O),请把下图中该反应的微观粒子补画齐全_____。
2 N2 + 6 H2O),请把下图中该反应的微观粒子补画齐全_____。
(2)可燃物在有限空间里极速燃烧可导致爆炸,下列混合物遇明火不会发生爆炸的是_____(填字母序号)。
a.沼气和空气 b.N2和O2 c.CO和O2 d.H2和O2
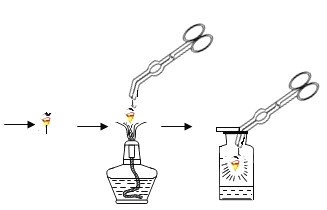
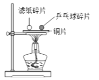
(3)灭火方式有多种,图乙、图丙灭火原理不同点在于_____。若在家里炒菜遇到油锅着火,适合使用的灭火方法是_____。
【答案】使装置密闭,防止生成的五氧化二磷(可吸入颗粒物)逸散到空气中 a、c 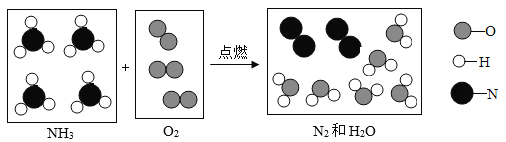 b 乙:降低温度至着火点以下 丙:隔绝氧气 锅盖盖灭
b 乙:降低温度至着火点以下 丙:隔绝氧气 锅盖盖灭
【解析】
(1)① 甲实验中气球的作用是使装置密闭,防止生成的五氧化二磷(可吸入颗粒物)逸散到空气中;a处与氧气接触的白磷燃烧,c处不与氧气接触的白磷不燃烧,通过观察a、c处的现象,可得出燃烧需要氧气的结论;
② 根据质量守恒定律可知,反应前后原子的种类、个数、质量不变,氨气在纯氧气中也能燃烧,方程式:4 NH3 + 3 O2  2 N2 + 6 H2O),该反应的微观粒子应补充三个氧分子和2个水分子、两个氮分子;
2 N2 + 6 H2O),该反应的微观粒子应补充三个氧分子和2个水分子、两个氮分子;
(2)可燃物在有限空间里极速燃烧可导致爆炸,
a.沼气和空气,沼气的主要成分是甲烷,在空气中能燃烧,可能引发爆炸;
b.氮气不可燃,N2和O2 的混合物不会发生爆炸;
c.一氧化碳可燃,CO和O2的混合物燃烧可能引发爆炸;
d.氢气可以燃烧,H2和O2的混合物燃烧可能引发爆炸;故选b;
(3)灭火方式有多种,图乙、图丙灭火原理不同点在于图乙中是采用降低温度至可燃物的着火点以下的方法,图丙采用的是隔绝氧气的方法;若在家里炒菜遇到油锅着火,适合使用的灭火方法用锅盖盖灭(隔绝氧气)。

 每课必练系列答案
每课必练系列答案【题目】人体缺铁时会得贫血症,如图是铁在元素周期表中的相关信息。下列说法正确的是( )
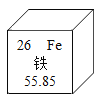
A.铁原子的质子数为26
B.铁是地壳中含量最高的金属元素
C.铁原子的相对原子质量是55.85g
D.铁属于非金属元素
【题目】测定黄铜(铜锌合金)中铜的质量分数的过程如下,请回答下列问题:
(1)小华同学取50 g黄铜,加入足量稀硫酸,共收集到1.0 g气体,计算黄铜中铜的质量分数______________(写出计算过程)。
(2)小婷同学另取50 g黄铜于烧杯中,将600 g稀硫酸分六次加入,测得加入稀硫酸的质量和烧杯中剩余物的质量如下表:
次数 | 一 | 二 | 三 | 四 | 五 | 六 |
加入稀硫酸的质量 / g | 100 | 100 | 100 | 100 | 100 | 100 |
烧杯中剩余物的质量 / g | 149.8 | a | 349.4 | 449.2 | 549.0 | 649.0 |
① 表中a = _____。
② 第六次实验后所得溶液的溶质是_____(写化学式)。
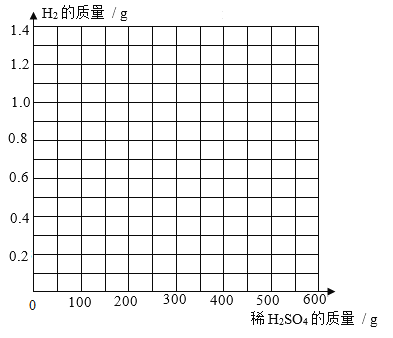
③ 画出加入0~600 g稀硫酸过程中生成H2质量的变化图,并标注必要的数值_____。
【题目】在一定条件下,甲、乙、丙、丁四种物质在一密闭容器中充分反应,测得反应前后各物质的质量如表所示。根据表中信息判断下列说法正确的是
物 质 | 甲 | 乙 | 丙 | 丁 |
反应前的质量 | 2 | 30 | 20 | 10 |
反应后的质量 | m | 39 | 5 | 16 |
A.该反应是化合反应B.甲一定是该反应的催化剂
C.反应过程中乙、丙变化的质量比为3:5D.丙可能是单质
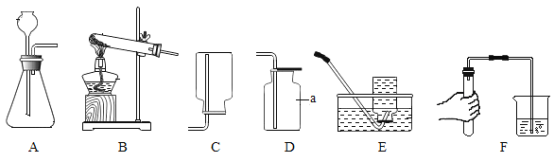
【题目】下列对比实验中能达到实验目的,且实验现象正确的是
选项 | A | B | C | D |
实验示意图 |
|
|
|
|
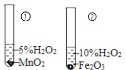
实验目的 | 探究过氧化氢溶液的浓度对反应速率的影响 | 证明二氧化碳与水反应生成了碳酸 | 区分硬水和软水 | 探究燃烧的条件之一是温度达到可燃物的着火点 |
实验现象 | ②比①反应速率快 | ①不变红,②变红 | 硬水中浮渣较多,软水中浮渣较少 | 滤纸碎片比乒乓球碎片先燃烧 |
A.AB.BC.CD.D