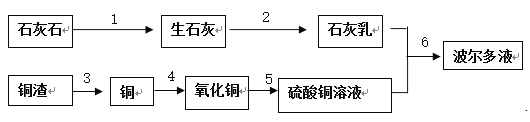
【题目】测定合金中铜的质量分数。为测定某铜、锌合金中铜的质量分数,兴趣小组同学称取20g合金于烧杯中,将80g稀盐酸分四次加入,充分反应,测得实验数据如下表所示:
第一次 | 第二次 | 第三次 | 第四次 | |
加入稀盐酸的质量(g) | 20 | 20 | 20 | 20 |
烧杯中剩余物的质量(g) | 39.92 | 59.84 | 79.80 | 99.80 |
(1)该铜、锌合金中铜的质量分数为_____________? (写出计算过程)
(2)第三次加入稀盐酸后烧杯内溶液中的溶质为________________(写化学式)。
【题目】探究氢氧化钠与二氧化碳的反应化学课上各小组的同学进行了如图所示实验:将二氧化碳通入氢氧化钠溶液中,没有观察到明显现象。
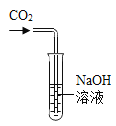
(定性实验)
(1)甲组同学为确定反应后所得溶液中溶质的成分,进行了如下探究:
实验步骤及现象 | 实验结论 |
______________________。 | 反应后溶液中的溶质为碳酸钠和氢氧化钠 |
(分离提纯)
(2)乙组同学欲从反应后所得的氢氧化钠和碳酸钠的混合液中提纯氢氧化钠固体,请将下表填写完整
选用的仪器名称 | 实验步骤 |
______________________。 | ______________________。 |
(定量实验)
(3)小组同学继续对一瓶长期放置的氢氧化钠固体的成分进行探究,利用化学沉淀法定量测量固体中氢氧化钠的含量,请你设计一套方案。你选择的反应原理是(用化学反应方程式表示)_______________________。
1试将实验操作流程补充完整(试剂任选),操作流程按下列图示表述:
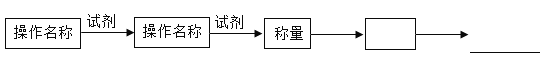
操作流程为:_______________________
2实验时称量样品的质量为a克,所测物质的质量为b克,则该试样中Na2CO3纯度的表达式为:___________________。
(反思交流)
(4)小组同学查阅了20℃时NaOH、Na2CO3在水中和乙醇中的溶解度
物质 | 20℃时的溶解度(g) | |
水 | 乙醇 | |
氢氧化钠 | 109 | 17.3 |
碳酸钠 | 21.8 | <0.01 |
经讨论,小组同学认为可以利用以上信息设计实验,通过观察明显现象证明CO2确实与NaOH发生了化学反应。他们的实验方案是_________________________________,实验过程中发生反应的化学方程式为________________________________________。