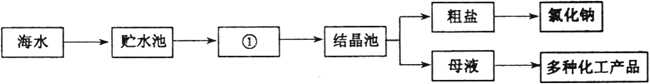
【题目】除去下列各特质中的少量杂质,所有除杂试剂及操作方法均正确的是
特质 | 杂质(少量) | 加入试剂及用量 | 除杂操作方法 | |
A |
|
| 过量的 | 过滤,除去滤渣 |
B |
|
| 过量的稀硫酸 | 过滤,洗涤、干燥滤渣 |
C |
|
| 过量的铜粉 | 过滤,洗涤、干燥滤渣 |
D |
|
| 过量的氧化铜 | 加热 |
A. AB. BC. CD. D
【题目】Na2CO3和NaHCO3有很多相似的化学性质,例如它们都能与稀盐酸反应生成_____气体。某学习小组对它们的鉴别方法产生了探究兴趣。
(提出问题)如何鉴别Na2CO3和NaHCO3呢?
(查阅资料)(1)NaHCO3固体受热分解生成碳酸钠和两种氧化物。
(2)Ca(HCO3)2可溶于水。
(3)通常状况下,NaHCO3是一种白色晶体,溶解度小于Na2CO3的溶解度,饱和的Na2CO3溶液中通入CO2气体,可生成NaHCO3。
(作出猜想)猜想一:可用酚酞溶液鉴别Na2CO3和NaHCO3溶液。
猜想二:可用加热的方法鉴别Na2CO3和NaHCO3固体。
猜想三:可用澄清石灰水鉴别Na2CO3和NaHCO3溶液。
猜想四:可用CO2气体鉴别Na2CO3和NaHCO3溶液。
小组同学一致认为猜想一不正确,理由是_____。
(实验探究)请你与小组同学一起探究。
实验操作 | 实验现象 | 实验结论 | |
实验1 | 分别取少量的Na2CO3和NaHCO3 固体于试管中加热,并将产生的气体通入澄清石灰水 | 加热Na2CO3时,澄清石灰水无变化;加热NaHCO3时,澄清石灰水变浑浊 | _____ |
实验2 | 分别取少量Na2CO3和NaHCO3溶液于试管中,加入澄清石灰水 | 两支试管中均产生了白色沉淀 | 猜想三 不正确 |
实验3 | 往盛有饱和Na2CO3和NaHCO3溶液的两支试管中分别通入足量的CO2气体 | 观察到_____ | 猜想四 正确 |
(问题讨论)
同学们对实验2的实验现象进行分析。从物质在溶液中解离出不同离子的微观角度分析,Na2CO3溶液与澄清石灰水发生反应的本质原因是_____,该反应的基本类型是_____。石灰水与NaHCO3溶液也能反应生成白色沉淀,老师指出其反应原理较复杂,有待于今后学习中进一步探究。
(拓展应用)
除去固体Na2CO3中混有的少量NaHCO3,可用的方法是_____(用化学方程式表示)。