题目内容
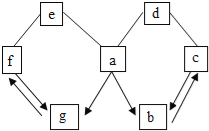
【题目】如图所示a﹣g是初中化学常见的物质.图中“→”表示转化关系,“﹣”表示相互能反应.已知a是人体胃液中含有的酸,g是最轻的气体,b、c、d、e、f都是氧化物.以下说法不正确的是( )
A. g是理想的燃料
B. e与f发生的化学反应类型是化合反应
C. b和c物质中所含元素相同
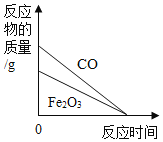
D. c、d发生反应的化学方程式只能是3CO+Fe2O3![]() 2Fe+3CO2
2Fe+3CO2
【答案】D
【解析】试题分析:a是人体胃液中含有的酸,可知a是盐酸,g是最轻的气体,可知g是氢气,a可以转化成b,b是氧化物,故可以想到由盐酸转化成的氧化物为二氧化碳,b.c之间又能互相转化,c也是氧化物,可以想到与二氧化碳可以互相转化的氧化物为一氧化碳,故c为一氧化碳,d是能与盐酸反应,又能与一氧化碳反应的氧化物,所以d可以是氧化铜等金属氧化物,f也是氧化物,他又能和氢气互相转化可以想到f是水,e能与水反应,还能与盐酸反应可以想到e为氧化钙,各种物质都推出来了,故不正确的叙述为D

 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案【题目】在研究酸和碱的化学性质时,某小组想证明稀硫酸和氢氧化钠溶液混合后,虽然无明显现象,但确实发生了化学反应。试与他们一起完成实验方案的设计、实施和评价,并得出有关结论。
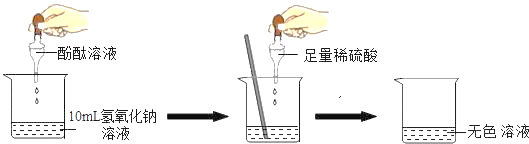
(1)如图所示,探究稀硫酸和氢氧化钠溶液的反应。当在NaOH溶液中滴入几滴酚酞试液后,溶液由无色变为_____色。根据上述实验中颜色变化,可确定稀硫酸和氢氧化钠溶液发生了化学反应,反应的化学方程式为_____。
(2)探究上述稀硫酸和氢氧化钠溶液反应后烧杯中的硫酸是否过量。根据上述反应过程中溶液变成无色,不能确定稀硫酸是否过量。同学们又分别选取氯化钡溶液、紫色石蕊试液设计实验方案,请你判断并
实验方案 | 实验步骤 | 实验现象 | 实验结论 |
方案一 | 取样,滴入适量的氯化钡溶液 | 出现白色沉淀 | 稀硫酸过量 |
方案二 | 取样,滴入几滴紫色石蕊试液 | 溶液变红 | 稀硫酸过量 |
方案三 | 取样,_____ | _____ | 稀硫酸过量 |
①上述设计的实验方案中,正确的是_____(填“方案一”或“方案二”);
②另外一个实验方案错误的原因是_____。
③完成方案三中实验步骤和现象,填写到表格中。
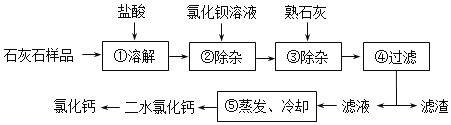
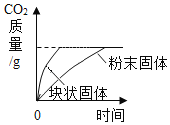
【题目】某化学小组对石灰石灼烧后得到的固体进行相关探究。
成分分析
(1)检验灼烧过程中产生的新物质
①根据已有知识和经验判断:石灰石灼烧后固体中含有CaO,判断的依据是_____(用化学方程式表示)。
②设计实验方案进行验证:
实验内容 | 实验现象 | 实验分析 |
取灼烧后固体放入盛有冷水的烧杯中,充分搅拌静置后,取少量上层澄清的液体置于试管中,向其中滴加2滴酚酞试液 | 溶液由无色变为_____色 | 反应后生成碱,请写出该反应的化学方程式:_____ |
(2)检验灼烧后固体中是否含有CaCO3
向盛有灼烧后固体的烧杯中滴加稀盐酸,有气泡产生,证明_____。
数据分析
用反应前后质量差计算灼烧后固体中CaCO3的质量分数
化学小组设计以下两个实验方案,方案中反应前后质量差分别用m1与m2表示。(两方案中实验操作误差忽略不计,取用的灼烧后固体成分均匀、质量相等,固体中除CaO、CaCO3其余成分均不发生反应,所用稀盐酸经估算确保足量)
实验方案 | 数据测量 | 数据处理 | |
反应前 | 反应后 | 反应前后质量差 | |
方案一:取灼烧后固体放入烧杯中,加入稀盐酸充分反应,不再产生气泡 | 灼烧后固体的质量、所用稀盐酸质量 | 烧杯中剩余物质的质量 | m1 |
方案二:取灼烧后固体继续灼烧,至固体的质量不再改变 | 灼烧后固体的质量 | 剩余固体的质量 | m2 |
结合信息,比较m1与m2的关系。请写出两种不同猜想并分别说明理由。
猜想1及理由:_____。
猜想2及理由:_____。
经分析选择合理的实验方案,进行计算……
拓展研究
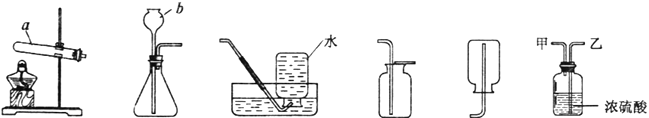
如图的酒精灯和酒精喷灯是常用的加热仪器,请回答下列问题:
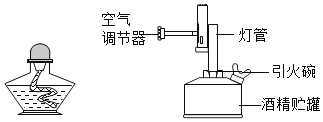
(1)酒精灯是玻璃仪器,火焰温度通常可达300~500℃,_____(填“焰心“、“内焰”或“外焰”)温度最高。熄灭酒精灯的方法是_____,采用此方法灭火的原理是_____。
(2)酒精喷灯一般是铜质仪器,火焰温度通常可达800﹣1000℃.使用酒精喷灯时应先向引火碗内注入![]() 容量的酒精,用火柴将引火碗内酒精点燃,点燃引火碗内酒精的目的是_____、_____。
容量的酒精,用火柴将引火碗内酒精点燃,点燃引火碗内酒精的目的是_____、_____。