题目内容
【题目】利用数据传感技术可以探究影响化学反应速率的因素。倾斜锥形瓶,使试管内稀盐酸流入瓶中与碳酸钙发生反应,测得瓶内气压随时间的变化如图所示。
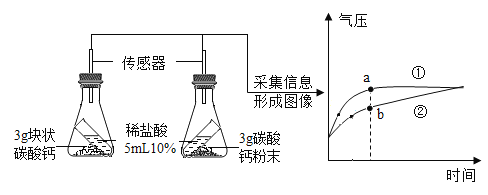
(1)写出锥形瓶中发生反应的化学方程式_____。
(2)哪条曲线表示的是碳酸钙粉末与稀盐酸反应?_____。
(3)对比分析a、b点可知,化学反应速率与什么因素有关?(写一条即可)_____。
【答案】CaCO3+2HCl=CaCl2+H2O+CO2↑ ① 反应物的接触面积
【解析】
(1)碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑。
(2)对比分析a、b点可知,曲线①单位时间内气压大,说明单位时间内产生的气体多,反应速率快,曲线①表示粉末状碳酸钙与稀盐酸反应,②表示块状碳酸钙与稀盐酸反应。
(3)对比分析a、b点可知,曲线①单位时间内气压大,说明单位时间内产生的气体多,反应速率快,曲线②表示粉末状碳酸钙与稀盐酸反应,说明化学反应速率与反应物的接触面积有关。

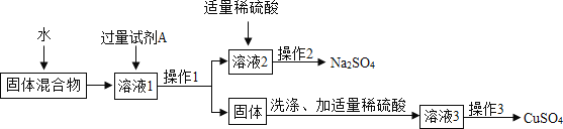
【题目】某化学实验室用稀硫酸处理含有氢氧化钠的废水。现取废水样品80g倒入烧杯中,加入几滴无色酚酞溶液,然后逐滴加入9.8%的稀硫酸,反应过程中溶液的pH变化如图所示。
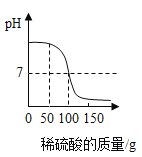
(1)当恰好完全反应时,溶液的颜色变化是____________。
(2)求废水中氢氧化钠的质量分数_______ (写出计算过程)。
(3)往上述80g废水中逐渐加入稀硫酸至过量,请在答题卡中画出Na2SO4质量随加入稀硫酸质量变化的曲线_______。
(4)下表为市面上浓硫酸和浓盐酸的有关数据:
物质 | 纯度 | 价格(元/kg) |
浓硫酸(工业级) | 98% | 0.6 |
浓盐酸(工业级) | 98% | 0.4 |
若工厂每天需处理上述废水8吨,选用__________(填“浓硫酸”或“浓盐酸”)更合算,每天可节约________元(保留整数)。
【题目】请根据下列实验装置图回答问题:

(1)写出仪器的名称①:____________;②_____________。
(2)实验室制取二氧化碳可选择的装置是___________,反应原理是__________________(用化学方程式表示),收集装置不能用C的原因是_________。
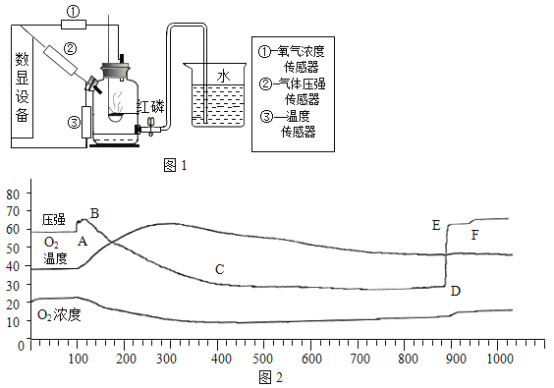
(3)实验室用高锰酸钾制取氧气时,要选用A装置,试管口略向下倾斜的目的是防止试管口的冷凝水回流到试管底部,炸裂试管。同学们对水的来源产生了兴趣,进行了如下探究。
[提出问题]试管口的水来自哪里?
[猜想与假设]
猜想1:高锰酸钾分解产生的水
猜想2:试管内空气中的水蒸气
猜想3:高锰酸钾固体含有水分
小莉认为猜想1不正确,理由是_________________。
[实验验证]同学们设计了以下方案进行验证。
实验方案 | 实验操作 | 实验现象 | 实验结论 |
方案一 | 用A装置,不加药品加热一段时间 | __________ | 猜想2不成立 |
方案二 | 将高锰酸钾先在酒精灯上加热干燥,再用A、C装置进行实验 | __________ | 猜想3成立 |
[交流与评价]方案二中先将高锰酸钾在酒精灯上加热干燥的目的是_____________。
[拓展延伸]实验室的化学试剂多数需要密封保存。下列实验室试剂要密封保存的目的正确的______________。
A纯碱密封保存防止与空气中的二氧化碳反应而变质
B白磷密封存于水中,防止发生自燃
C浓盐酸密封保存防止吸收空气中的水分使其浓度降低
【题目】化学物质之间的反应奥妙无穷。在一次化学探究活动中,同学们从不同角度对稀盐酸与氢氧化钠溶液的反应进行了探究:
(1)探究稀盐酸与氢氧化钠溶液发生了反应,同学们设计了实验方案一:
实验步骤 | 实验现象 | 结论 |
取少量稀盐酸,先用pH试纸测定稀盐酸的pH,再逐渐滴加氢氧化钠溶液,并不断振荡,同时测定混合液的pH. | pH逐渐变大至pH=7,最后pH>7 | 稀盐酸与氢氧化钠溶液能发生反应 |
①请你分析上述方案中为什么强调只有测得的pH=7,最后pH>7才能证明反应发生了?______。
②写出稀盐酸与氢氧化钠溶液反应的化学方程式______。
(2)探究稀盐酸与氢氧化钠溶液反应是放热的,同学们设计了实验方案二:
取20℃时的NaOH溶液10mL于烧杯中,逐滴滴入稀盐酸,然后用温度计测量溶液温度。随着盐酸的加入,烧杯中溶液温度与加入盐酸体积之间的变化关系如图一所示:
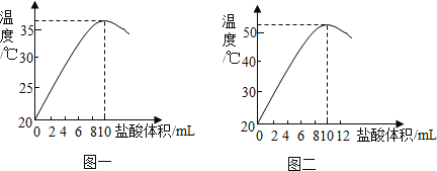
①滴加至8mL时,充分搅拌后滴入紫色石蕊试液,溶液呈______色,盐酸滴加至______mL时,溶液呈中性。
②继续滴加盐酸,溶液的温度下降的原因是______。是否可以用NaOH固体代替氢氧化钠溶液探究中和反应是否放热?______(填“是”或“否”)。
(3)小强同学对方案二的实验有异议,他找到了前几天所做的实验数据记,图二是烧杯中溶液温度与加入盐酸体积之间的变化关系图,造成两位同学所测溶液温度有差异的原因可能是:①______,②______。