题目内容
【题目】化学兴趣小组的同学将足量的锌粒加入到浓硫酸中,发现有大量的气泡放出,他们对气体的成分进行了探究。
(提出问题)锌粒加入浓硫酸后生成的气体是什么?
(查阅资料)①浓硫酸能与锌反应,但不产生氢气,也不会产生氧气;
②SO2有刺激性气味,易溶于水,能使品红(一种红色色素)溶液褪色;
③SO2、CO2与氢氧化钠溶液反应原理相同,且反应前后硫元素化合价不变。
(提出猜想)甲:气体是H2;
乙:气体是:SO2;
丙:气体是_____。
(实验探究)为了验证上述猜想,同学们在老师的指导下设计了如图的装置(部分夹持器材略去,假设每个能发生的反应都完全进行)进行探究:
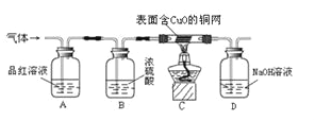
(1)实验开始后,观察到A中品红溶液褪色,证明气体中含有_____。
(2)B装置的作用利用了浓硫酸的_____性。
(3)C装置在点燃酒精灯加热之前应先通一段时间的气体,目的是_____,加热一段时间后,观察到_____的现象,证明气体中含有H2。
(4)D装置的目的是吸收尾气中的SO2,防止造成空气污染。请你写出D瓶中发生反应的化学方程式_____。
【答案】气体是气体是SO2和H2 二氧化硫 吸水性 排出玻璃管中的空气 黑色固体变成红色 SO2+2NaOH═Na2SO3+H2O
【解析】
[提出猜想]化学反应遵循质量守恒定律,即反应前后元素种类不变,所以丙:气体是气体是SO2和H2;
[实验探究](1)二氧化硫能使品红溶液褪色,所以实验开始后,观察到A中品红溶液褪色,证明气体中含有二氧化硫;
(2)浓硫酸具有吸水性,所以B装置的作用是吸收水蒸气;
(3)氢气与空气混合在加热时可能出现爆炸,氢气能与氧化铜反应生成铜和水,所以装置在点燃酒精灯加热之前应先通一段时间的气体,目的是:排出玻璃管中的空气,加热一段时间后,观察到黑色固体变成红色固体,玻璃管内壁出现水珠,证明气体中含有氢气,这是因为氢气能和氧化铜反应生成铜和水;
(4)二氧化硫和氢氧化钠反应生成亚硫酸钠和水,化学方程式为:SO2+2NaOH═Na2SO3+H2O。

【题目】某小组同学为探究二氧化锰对过氧化氢分解速度的影响,设计了以下实验:
(1)完善实验一、实验二:
实验步骤 | 实验现象 | 实验结论 | |
实验一 |
| 带火星的木条不复燃 | 过氧化氢分解的速率较慢 |
实验二 |
| ___________ | ________ |
(2)实验三:待实验二结束,剩余的液体化学式为_____,倒出多余液体,继续向其中加入5%的过氧化氢溶液,实验现象为____________,得出结论__________,写出此时的反应方程式__________;
(3)实验四,实验之前称量加入二氧化锰的质量为m1,待实验三结束后,取出二氧化锰,干燥后称量质量为m2,则m1_____m2(填“>”、“<”、“=”),得出结论___________,从液体中取出二氧化锰的操作名称为______;