题目内容
【题目】某化学小组向一定量AgNO3和Al(NO3)3的混合溶液中加入锌、铜粉末进行了如图实验. 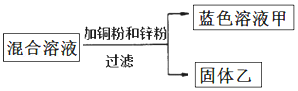
(1)向固体乙上滴加盐酸时(填“有”或“没有”)气泡产生;
(2)溶液甲中可能含有的溶质是(写化学式).
【答案】
(1)没有
(2)AgNO3
【解析】解:在金属活动性顺序中,由于金属的活动性是Al>Zn>H>Cu>Ag,向一定量的AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉的混合物,锌能与硝酸银反应生成硝酸锌和银,不能与硝酸铝反应,当锌粉反应完全后,铜能与硝酸银反应生成了硝酸铜和银,不能与硝酸铝反应.又因为溶液甲呈蓝色,说明滤液中还一定含有硝酸铜;(1)因为有硝酸铜的存在,因此就不会有比铜活动性强的锌剩余,因此过滤、洗涤后往固体乙中加入稀盐酸,没有气泡产生;(2)溶液甲中含有没参加反应的硝酸铝,反应产生的硝酸锌,硝酸铜,可能有硝酸银,溶液甲中可能含有的溶质是:AgNO3故答为:(1)没有;(2)AgNO3 .
【考点精析】本题主要考查了金属材料的选择依据的相关知识点,需要掌握黑色金属:通常指铁、锰、铬及它们的合金.重金属:如铜、锌、铅等;有色金属轻金属:如钠、镁、铝等;有色金属:通常是指除黑色金属以外的其他金属才能正确解答此题.

 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案【题目】工业铁红的主要成分是Fe2O3 , 还含有少量的FeO、Fe3O4 . 为了测定铁红中铁的质量分数,兴趣小组的同学进行了如下实验,请你参与过程分析.
【资料1】草酸晶体(H2C2O43H2O)在浓H2SO4作用下受热分解,化学方程式为:
H2C2O43H2O ![]() CO2↑+CO↑+4H2O
CO2↑+CO↑+4H2O
(1)下列可用作草酸分解制取气体的装置是(填字母编号). 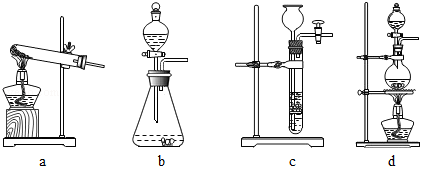
(2)【问题讨论】用图所示装置进行实验: 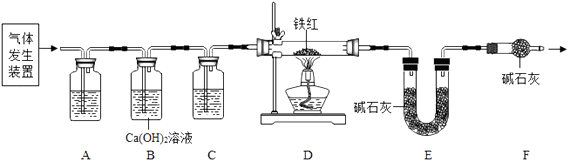
实验前应先 .
(3)进入D中的气体是纯净、干燥的CO,则A、C中的试剂依次是、(填字母编号). a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液
(4)B装置的作用是 .
(5)对D装置加热前和停止加热后,都要通入过量的CO,其作用分别是: ①加热前 . ②停止加热后 .
(6)写出D装置中所发生反应的一个化学方程式 .
(7)【数据分析与计算】【资料2】铁的常见氧化物中铁的质量分数:
铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
铁的质量分数 | 77.8% | 70.0% | 72.4% |
称取铁红样品10.0g,用上述装置进行实验,测定铁红中铁的质量分数.
①D中充分反应后得到Fe粉的质量为m g,则<m< .
②实验前后称得E装置增重6.6g,则此铁红中铁的质量分数是 .
【实验评价】
反思1:本实验中如果缺少C装置(不考虑其它因素),则测得样品中铁的质量分数会(填“偏小”、“不变”或“偏大”).
反思2:请指出【问题讨论】中实验装置的一个明显缺陷 .
