题目内容
【题目】如图是对能够生成氯化镁的反应进行的归纳与整理,请回答下列问题: 
(1)反应④中各元素化合价(选填“变”或“不变”);
(2)若Y是一种盐,请写出Y中阳离子符号;
(3)写出物质Z的化学式;
(4)完成③的化学方程式 .
【答案】
(1)不变
(2)Cu 2+或者Fe 2+
(3)MgSO4
(4)Mg(OH)2+2HCl=MgCl2+2H2O
【解析】解:(1)反应④,是碳酸镁和盐酸反应,生成氯化镁和水以及二氧化碳,反应类型是复分解反应,复分解反应的特点是“两相换价不变”,也就是复分解反应中各元素化合价不变;(2)反应⑤是镁和某种物质反应生成氯化镁,所以应该是镁和金属活动性排在镁后面的金属对应的可溶性盐溶液,所以Y中阳离子符号 Cu 2+或者Fe 2+等;(3)⑥是物质氯化钡和某种物质反应生成氯化镁,由于氯化镁可溶,所以只能是对应生成物为难溶性钡盐,为碳酸钡或者硫酸钡钡盐,由于碳酸镁不溶,硫酸镁可溶,根据复分解反应的条件“有酸可不溶,无酸需都溶”,z只能是硫酸镁,对应的Z的化学式 MgSO4;(4)③是酸和碱反应生成氯化镁,所以应该是氢氧化镁和盐酸反应生成氯化镁和水,对应的化学方程式 Mg(OH)2+2HCl=MgCl2+2H2O. 所以答案是:(1)不变;(2)Cu 2+或者Fe 2+;(3)MgSO4;(4)Mg(OH)2+2HCl=MgCl2+2H2O.
【考点精析】利用金属材料的选择依据和书写化学方程式、文字表达式、电离方程式对题目进行判断即可得到答案,需要熟知黑色金属:通常指铁、锰、铬及它们的合金.重金属:如铜、锌、铅等;有色金属轻金属:如钠、镁、铝等;有色金属:通常是指除黑色金属以外的其他金属;注意:a、配平 b、条件 c、箭号.

【题目】某化学小组向一定量AgNO3和Al(NO3)3的混合溶液中加入锌、铜粉末进行了如图实验. 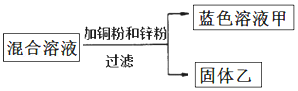
(1)向固体乙上滴加盐酸时(填“有”或“没有”)气泡产生;
(2)溶液甲中可能含有的溶质是(写化学式).
【题目】有关蜡烛及燃烧的实验探究:
实验现象 | 结论 |
把一只干燥的冷烧杯罩在酒精灯火焰上,观察到烧杯内壁出现水雾 | 说明酒精燃烧时生成了 |
用手触摸上一步骤中的烧杯底部,感觉 | 说明酒精燃烧时有热量放出 |
向上述烧杯中加入少量澄清石灰水振荡,发现石灰水变浑浊 | 说明酒精燃烧还生成了 |

