题目内容
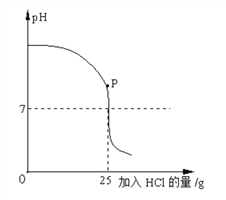
【题目】某兴趣小组的同学在帮老师整理实验室时发现一瓶脱落的氢氧化钠溶液,他们想知道该瓶氢氧化钠溶液的质量分数,于是他们取该氢氧化钠溶液20g,然后将18.25%的稀盐酸逐步加入,反应过程中溶液的pH变化如下图。
试回答:(1)在P点时,溶液中的溶质是: _____________________________;
(2)该氢氧化钠溶液中溶质的质量分数为_________。
【答案】 NaOH NaCl 25%
【解析】本题考查了反应后溶液的溶质的判定和根据化学反应方程式的计算。根据反应过程中溶液的pH变化判断反应的进程是解题的关键。
(1)由图像可知,P点时溶液的pH>7,溶液中存在反应生成的氯化钠(NaCl)和没有完全反应的氢氧化钠(NaOH);
(2)根据图像可知,25g的盐酸与20g的氢氧化钠溶液恰好完全反应。
设: 20g的氢氧化钠溶液中氢氧化钠的质量为x
HCl+ NaOH═NaCl+H2O
36.5 40
25g×18.25% x
![]() 解得:x=5g
解得:x=5g
氢氧化钠溶液中溶质的质量分数=![]() ×100%= 25%。
×100%= 25%。

练习册系列答案
相关题目