题目内容
【题目】47.2017年世界环境日中国的主题是“绿水青山就是金山银山”
(1) 减少污染物排放——空气清新
引起酸雨的主要物质是_________,低碳生活可以减缓________引起的温室效应。
(2)自来水来之不易——节约用水
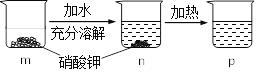
自来水生产流程: ![]() 通常加入__________吸附水中的异味和色素,氯气的作用是_________________。
通常加入__________吸附水中的异味和色素,氯气的作用是_________________。
(3)清洁高效能源——天然气
天然气的主要成分是甲烷,燃烧的化学方程式是_____________________________。
【答案】 SO2 CO2 活性炭 消毒 CH4 + 2O2 ![]() CO2 +2H2O
CO2 +2H2O
【解析】本题考查了自来水的生产过程与净化方法,二氧化碳对环境的影响,酸雨的产生,甲烷的燃烧。难度不大依据已有的知识进行分析。
(1)引起酸雨的主要物质是二氧化硫(SO2),低碳生活可以减缓二氧化碳(CO2)引起的温室效应;
(2)活性炭具有吸附性。自来水生产流程中通常加入活性炭吸附水中的异味和色素,氯气能杀死水中微生物,氯气的作用是消毒;
(3)甲烷与氧气在点燃的条件下生成水和二氧化碳,化学方程式是H4 + 2O2 ![]() CO2 +2H2O。
CO2 +2H2O。

【题目】某研究性小组对硫酸铵〔(NH4)2SO4〕化肥进行等级测定(该化肥中不存在其他含氮物质)。
【查阅资料】①氨气极易溶于水,其水溶液为氨水。氨水呈碱性,不稳定,易挥发。
②碱石灰是一种常见的干燥剂,其主要成分是CaO和NaOH固体混合物。
③硫酸铵化肥等级指标如下表:
指标项目 | 优等品 | 合格品 |
氮(N)含量 | ≥21.0% | ≥20.5% |
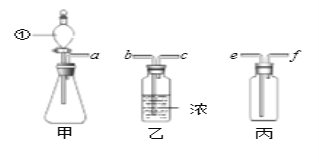
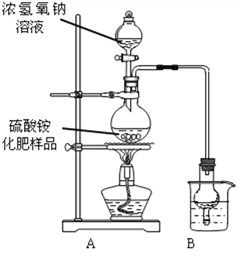
【实验设计】按右图所示装置进行实验。
(1)实验过程中,往烧瓶中加入足量浓氢氧化钠溶液,并加热使硫酸铵充分反应完全转化为NH3.
(2)B的作用是为了吸收产生的氨气。烧杯中最适宜的试剂是_________(填序号)
①水 ②浓HCl ③稀H2SO4 ④NaOH溶液
【交流讨论】实验小组同学认为用上述实验装置测得的硫酸铵化肥含氮量可能偏高,应在实验装置A、B之间增加一个装有______(填“浓硫酸”或“碱石灰”)的干燥装置。
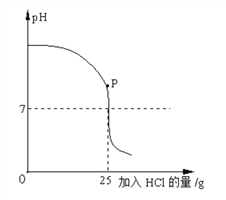
【实验测定】经讨论后,他们改进了实验装置,排除了可能产生误差的因素,重新进行实验。取硫酸铵化肥样品13.5g进行实验,测得B装置增重3.4g。请通过计算判断该化肥的等级。________(写出计算过程)
【题目】某研究性学习小组在验证“碱溶液使酚酞试液变红”的实验时,发现一个意外现象:将酚酞试液滴人某NaOH溶液中,溶液变成了红色,可是过一会儿红色却又消失了。
【提出问题】是什么原因导致滴有酚酞的NaOH溶液由红色褪为无色?
【猜想与假设】他们分别对这种意外现象作如下猜想:
甲同学:可能是酚酞与O2发生了反应;
乙同学:可能是NaOH溶液与空气中的CO2发生了反应;
丙同学:可能与NaOH溶液浓度大小有关;
【设计实验】三位同学分别设计实验验证自己的猜想:
(1)甲同学设计了如下实验,请你填写下表。
实验步骤 | 设计这一步骤的目的 | 实验现象 | 实验结论 |
1.将NaOH溶液加热煮沸 | _________ | 溶液变红,过一会儿红色消失 | 甲同学猜想不正确 |
2.向冷却后的溶液中滴人酚酞,并滴一些植物油在其上方 | _______ |
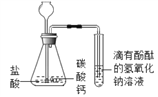
(2)乙同学设计如图装置进行实验,一段时间后,试管中溶液的红色褪去,于是认定自己的猜想正确。请写出CO2与NaOH溶液反应的化学方程式:_____。甲同学认为乙同学的实验不够严谨,理由是_____。
(3)请设计一个实验方案证明丙同学的猜想正确。___________(写出操作方案和现象)。