题目内容
【题目】固体酒精,因使用、运输和携带方便,燃烧时对环境的污染较少,与液体酒精比较安全性较高,作为一种固体燃料,广泛应用于餐饮业、旅游业和野外作业的等场合。在一次用餐中,同学们对固体酒精产生了好奇,于是对其成分进行研究。

(查阅资料)(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成。(2)氯化钙、氯化钡溶液均呈中性。(3)浓硫酸具有很强的吸水性;碱石灰常用于吸收水蒸气和二氧化碳。
探究活动一:探究固体酒精的成分
(提出问题)(1)酒精中是否含有碳元素?
(2)固体酒精中的氢氧化钠是否变质?
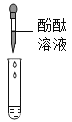
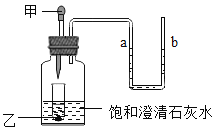
(实验探究)(1)按右图实验,发现澄清石灰水变浑浊,由此可得出酒精中含有碳元素的结论,此结论__________(选填“合理”或“不和理”)。

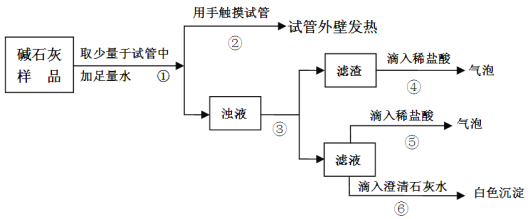
(2)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀,取沉淀与试管中加稀盐酸,有气泡产生,写出产 生气体的化学方程式:______________ 。分析实验并结合资料得出氢氧化钠已变质。
(3)为进一步确定氢氧化钠的变质程度,分组探究。
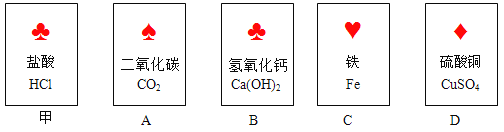
①甲组烧杯上层清夜于两支试管中,按下图探究。
方案 | | |
现象 | 溶液变红 | 产生 |
结论 | 清液中有氢氧化钠 | 清夜中有碳酸钠 |
②乙组认为甲组实验不能证明清夜中一定有氢氧化钠,理由与是_______________。他们另取烧杯中上层清夜,加足量氯化钡溶液,充分反应后滴加酚酞溶液,酚酞溶液变红。
(实验结论)经讨论一致认为固体酒精中的氢氧化钠部分变质。
(拓展应用)要除取部分变质的氢氧化钠溶液中的杂质,可选择适量的__________(选填字母序号)。
ABa(OH)2溶液 BCaCI2溶液 CCa(OH)2
探究活动二:探究固体酒精中碳酸钠的质量分数利用如图所示实验装置(铁架台略去)和试剂,通过测定样品和稀盐酸反应产生的CO2气体的质量,计算Na2CO3的质量分数(装置气密性良好,忽略盐酸的挥发性且每步反应或作用都是完全的)。
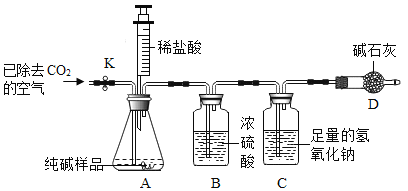
(1)打开止水夹K,先对装置A和B(已连接)通入已除去CO2的空气一会儿,以排尽装置的A和B中含有的__________,再接上装置C和D。
(2)关闭止水夹K,加入足量的稀盐酸(杂质不与盐酸反应)。
(3)待装置A中的反应结束后,再一次打开止水夹K,继续往装置通入已除去CO2的空气一会儿。根据质量守恒定律,装置_________(填序号)在反应前后的质量差就是产生CO2的质量,由此计算出该固体酒精中Na2CO3的质量分数。若没有装置D,将会使测定结果______________(选填“偏大”或“偏小”)。
【答案】合理 CaCO3+2HCl=CaCl2+CO2↑+H2O 碳酸钠溶液显碱性,也能使酚酞试液变红色 AC 二氧化碳 C 偏大
【解析】
解:探究活动一:(1)按右图实验,发现澄清石灰水变浑浊,说明酒精燃烧的产物中含有碳元素,根据质量守恒定律分析,可得出酒精中含有碳元素的结论;
(2)氢氧化钠能和空气中的二氧化碳反应生成碳酸钠和水,碳酸钠能和氯化钙反应生成碳酸钙沉淀和氯化钠,因此白色沉淀是碳酸钠和氯化钙反应生成的碳酸钙,碳酸钙和稀盐酸反应的化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O;
(3)碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠;乙组认为甲组实验不能证明清夜中一定有氢氧化钠,理由是:碳酸钠溶液显碱性,也能使酚酞试液变红色;
[拓展应用]要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的氢氧化钡溶液、氢氧化钙溶液,不能选择氯化钙溶液,因为碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,因此使用氯化钙时能够带入新杂质--氯化钠;
探究活动二:(1)空气中含有二氧化碳,所以打开止水夹K,先对装置A和B(已连接)通入已除去CO2的空气一会儿,以排尽装置A和B中含有的二氧化碳,再接上装置C和D;
(2)由质量守恒定律可知装置C中反应前后的质量差就是产生CO2的质量,装置D的作用是防止空气中的二氧化碳和水蒸气进入装置C,所以若没有装置D,将会使测定结果偏大。

 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
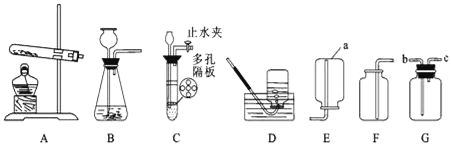
品学双优卷系列答案【题目】I以下是化学实验室内几种常用的实验装置,请回答:
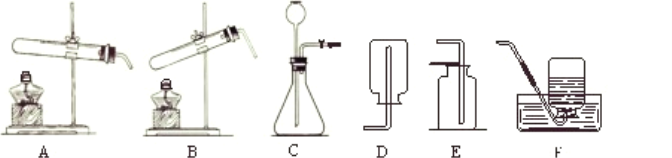
(1)某同学用A装置取并收集一瓶氧气,反应的化学反应方程式为______,采用排水集气法收集氧气不纯原因可能是____________。
(2)若用高锰酸钾制氧气,下列操作①点燃酒精灯,加热②检查装置气密性③装药品,固定装置④排水法收集气体⑤从水槽中取出导管⑥熄灭酒精灯⑦连接仪器,正确顺序是_______。(用序号表示)
(3)利用C装置可以完成实验室制取二氧化碳,写出相关反应化学方程式:___________
(4)若在常温下,用亚硫酸钠固体和稀硫酸制取二氧化硫气体,二氧化硫是易溶于水、密度比空气大的有毒气体,应选用的发生装置是_____ ;收集装置是_________。
Ⅱ某学生为了证明甲烷中含有碳、氢元素,设计并完成了如下实验,请补充完整。
实验步骤 | 实验现象 | 结 论 |
(1)先___________,点燃甲烷 (2)将光洁干燥的小烧杯罩在甲烷燃烧的火焰上方 | 现象______________ | 证明含有氢元素 |
(3)将蘸有澄清石灰水的小烧杯罩在甲烷燃烧的火焰上方 | 现象______________ | 证明含有碳元素 |
Ⅲ某校研究性学习小组用下图装置进行镁条在空气中燃烧的实验:
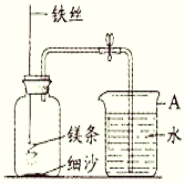
(1)镁条燃烧、冷却后打开止水夹,若弹簧夹未夹紧,则进入集气瓶中的水会偏_______。
(2)若镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的_____%。现进入集气瓶中水的体积约为其容积的70%,根据空气的组成可推出减少的气体中有氮气。
(发现问题)氮气是怎么减少的呢?
(推测一)氮气与镁条反应而减少;
(推测二)__________________
(查阅资料)
镁条还可以在二氧化碳中燃烧生成一种单质和一种金属氧化物,反应的方程式为___________