��Ŀ����
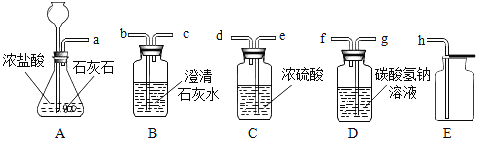
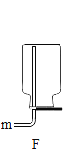
����Ŀ����ͼ�ǰ�������A��B��C��D�����ῨƬ������ѧƴͼ�����������ſ�Ƭ��������ʣ�������Һ�����ܷ�����Ӧ��

��1��A��������______�����ţ���
a Mg b Fe c Ag d Zn
��2����BΪ�������Ҫ�ɷ�Fe2O3��B�����ᷴӦ�Ļ�ѧ����ʽΪ________��
��3����CΪ����DΪ��ʯ�ң���C��D��Ӧ�Ļ�ѧ����ʽΪ__________��
��4����������̼ͨ��C��Һ���ɻ�������̼�����ƣ� NaHCO3�����÷�Ӧ�ķ�Ӧ����______�֡�
���𰸡�c Fe2O3+6HCl=2FeCl3+3H2O Ca(OH)2+Na2CO3=CaCO3��+2NaOH ��
��������
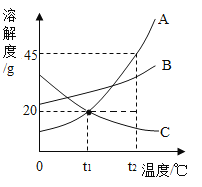
��1����ͼ��֪A�������ܷ�Ӧ��ֻ�����ڽ������˳������Ԫ�غ��棬�������Ӧ����ѡ��c��
��2�������������ᷴӦ�����Ȼ�����ˮ����ѧ����ʽΪFe2O3+6HCl=2FeCl3+3H2O�����Fe2O3+6HCl=2FeCl3+3H2O��
��3������Ϊ̼������ʯ��Ϊ�������ƣ�������Ӧ����̼��Ƴ������������ƣ���ѧ����ʽΪ��Ca(OH)2+Na2CO3=CaCO3��+2NaOH�����Ca(OH)2+Na2CO3=CaCO3��+2NaOH��
��4����������̼ͨ��̼������Һ�п�������̼�����ƣ���ѧ����ʽΪNa2CO3+CO2+H2O=2NaHCO3����Ӧ�������֣��������

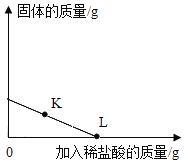
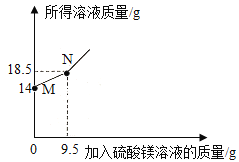
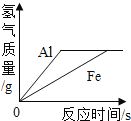
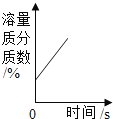
����Ŀ����ͼ��ʾͼ���У�����ȷ��ӳ��Ӧ�仯��ϵ����
A | B | C | D |
|
|
|
|
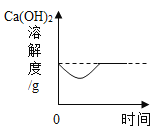
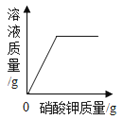
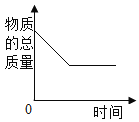
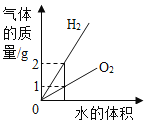
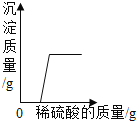
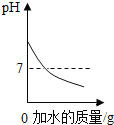
��ʯ��ˮ�м���һ����CaO | һ�����£������������Һ�м�������ع��� | һ�������ĺ������ܱ�������ȼ�� | ���ˮ������������������ |
A. A B. B C. C D. D
����Ŀ��ij�������÷������Ʊ�K2SO4����������:

���� | KCl | K2SO4 | NH4Cl | (NH4)2SO4 |
�ܽ��/g(20��C) | 34.2 | 11.1 | 37.2 | 75.4 |
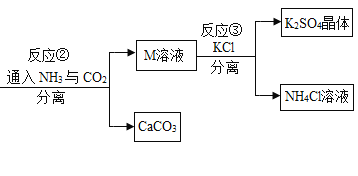
��1�������Ͻ�CaCO3�гɷ�ĩ��Ŀ����________________________________��
��2�����������У������ۺ�����CO2�⣬����ѭ��ʹ�õ�������______(�ѧʽ)��
��3��д����Ӧ�ڵĻ�ѧ����ʽ:___��
��4����Ӧ����������ʵ��ܽ�������ʾ����Ӧ���ڳ�������ʵ�ֵ�ԭ����____��
��5��ϴ�ӷ�Ӧ�����þ��岻��ˮ���ñ���K2SO4��Һ��Ŀ����_______������˾����Ƿ�ϴ���ķ�����_____��