��Ŀ����
����Ŀ��ij��ѧ��ȤС���ͬѧ��ѧϰ�˿��������������IJⶨ�Ļ����ϣ��Ľ��˽̲��е�ʵ�飬��Ƴ�����ͼ��ʾ��ʵ��װ�á�ʵ�鲽�����£�
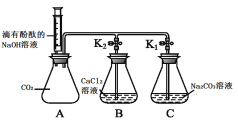
���������������װ�������ԣ�����װ�����������á�
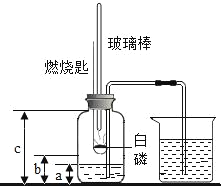
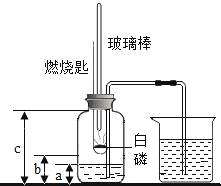
���ڼ���ƿ��װ������a�����ˮ��ȼ�ճ����һС����ף��ھƾ����ϰѲ������¶˼��ȣ���ͼʾ�Ѽ���ƿ�еĿ����ܷ��������Ѽ���ƿ�ڵij������쵽ƿ�ף������ܵ���һ�˷���ʢ������ˮ���ձ��С�
����Ԥ�ȼ��ȹ��IJ�������������Ӵ����۲쵽���������Ż�ȼ�ղ����������̣�ͬʱ���ȡ�
��������ȼ��Ϩ����Լ���������ʧ��
��������ƿ��ȫ��ȴ�����£���������ƿ��ˮ�����Ϊb����������ƿ�����Ϊc��
������a��b��c�������ݣ���������������������������
����������Ϣ���ش��������⣺
��1���ڰ���ʼȼ�յ����Ϩ��Ĺ����У�����ƿ��ˮ��ı仯�����_____��
��2����ʵ��ɹ�����д��a��b��c��������Ӧ�����һ����ʽ��ϵ_____��
��3��С���ԱС������䷢�ֲ���������ƿ�ڵ�ˮ�еμӼ���ʯ����Һ�����졣��һ����ʹ���ڳ�Ա�����ؿ�չ���ۣ�С����Ϊ�����ڶ�����̼����ˮ��ʹ��Һ�����ԣ���С�����Ϸ��ԣ������ж�����̼�ĺ������٣���ʵ������û�в���������̼����ʱ���ڲ�����ʹ��Һ�����ԡ��������ȷ�Ĺ۵㣬�Ա����������IJ��룺_____��
��4������ʵ���У�������ƿ�ڵĵ���û�б�Һ���ס�����²����Ľ����_____��ѡ�ƫ����ƫС�����䡱����
���𰸡����½������� c+4a��5b �����ǰ���ȼ�����ɵ���������������ˮ��������Һ�����ԣ���������������ˮ��Ӧ�����ᣩ ƫ��
��������
��1������ȼ��ʱ��ų��������ȣ�����ƿ�ڿ�������������ͣ���ѹ����ʹ����ƿ�ڵ�ˮ�ز����������ձ��ڣ�ȼ��ֹͣ���¶��½���ƿ����ѹ��С���ձ��е�ˮ�ͻ����Ų����������뼯��ƿ�ڣ��������½���������
��2����������ƿ�����Ϊc������ƿ��װ������a�����ˮ�����Լ���ƿ�п��������Ϊ��c��a������������Լռ������������֮һ����ʵ��ɹ�����b��a������c��a����1/5����c+4a��5b������c+4a��5b��
��3�������ǰ���ȼ�����ɵ���������������ˮ�����ԣ��μӼ�����ɫʯ����Һ����Һ���죬��������ǰ���ȼ�����ɵ���������������ˮ��������Һ�����ԣ���������������ˮ��Ӧ�����ᣩ��
��4���������ܵ��¶�û�б�ˮҺ�⣬����ȼ�շų������ᵼ�¼���ƿ�ڵĿ����������ͣ�һ���������ݳ�������ɲ���ֵƫ����ƫ��

 ��ĩ100�ִ��غ�������ϵ�д�
��ĩ100�ִ��غ�������ϵ�д� Сѧ�������Ծ�ϵ�д�
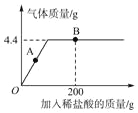
Сѧ�������Ծ�ϵ�д�����Ŀ����һ����ij��������μ���ij��Һ��������x���ʾ������Һ������������ѡ����y���ʾ�ĺ���������ͼ��仯����һ�µ��ǣ�������
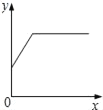
ѡ�� | �� �� | �� Һ | y �� �� �� |
A | �������� | ����������Һ | ˮ������ |
B | ����ʯ�����ʲ���Ӧ�� | ϡ���� | ���������ʵ��������� |
C | ������ͭ�ۻ�Ϸ�ĩ | ����ͭ��Һ | ������Һ������ͭ������ |
D | �Ȼ�����̼���ƻ�Ϸ�ĩ | ϡ���� | ������̼����� |
A. AB. BC. CD. D
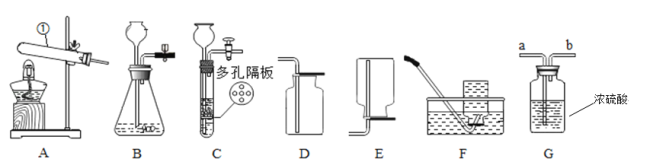
����Ŀ��Ϊ̽������Ļ�ѧ���ʣ�ij��ѧС����������ʵ�飺
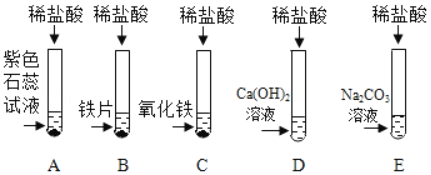
(1)A�Թ��е�ʵ������Ϊ_____��C�Թ�����������Ӧ�Ļ�ѧ����ʽΪ_____��
(2)����Ӧ��D��E�Թ��еķ�Һ����һ���ྻ���ձ��У��۲쵽�ձ����������ݲ��������а�ɫ�������֡����ձ��еĻ������ˣ��õ���ɫ��������ɫ��Һ��ͬѧ�Ƕ���Һ�����ʵijɷֽ���̽����
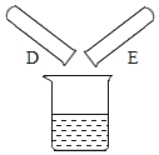
��������⣩��Һ�����ʵijɷ���ʲô��
���������룩���룺NaCl
�������NaCl��CaCl2
��������_____
�����ģ�NaCl��Ca(OH)2��HCl
���������ۣ��������ۣ�ͬѧ��һ����Ϊ����_____�Ǵ���ġ�
�����ʵ�飩�����ʵ�鱨�档
ʵ�鲽�� | ʵ������ | ʵ����� |
ȡ������Һ���Թ��У��μ�������̼������Һ�� | _____ | ����������� |
ȡ������Һ���Թ��У��μ�_____(������)�� | _____ | ���������� |
��Ǩ����չ��ϡ���ᡢϡ������һЩ���ƵĻ�ѧ���ʣ�����Ϊ�ڲ�ͬ������Һ�ж�����_____��