题目内容
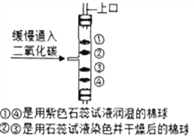
【题目】如图是测定空气中氧气含量的实验装置图.所示实验中,实验步骤如下(装置气密性良好,部分操作已略去)

I.打开止水夹a和b,向集气瓶中缓慢鼓入一定量空气,至白磷与空气接触,测得进入量筒中水的 体积为V1; II.强光照射引燃白磷; III.白磷熄灭并冷却至室温,测得量筒中的体积变为V2; Ⅳ.计算空气中氧气的体积分数.
下列有关这个实验的说法中,正确的是( )
①步骤I中,俯视量筒读数会使测得的V1数值偏低;
②步骤II中,白磷燃烧时可以不关闭止水夹a和b;
③步骤III中,未冷却至室温会使测得的V2数值偏高;
④步骤IV中,求得氧气的体积分数等于![]() ×100%
×100%
A. ①②③④ B. ②③ C. ③④ D. ①③④
【答案】C
【解析】①读取液体体积时,视线应与凹液面的最低处保持水平,仰视读数偏大,俯视读数偏小,错误;②步骤II中,白磷燃烧会放出热量导致瓶内的空气膨胀,不关闭止水夹a和b会导致出现误差,错误;③步骤III中,未冷却至室温时瓶内的压强变化不大,会导致进入瓶内的水的体积偏小,即会使测得的V2数值偏高,正确;④空气中氧气的体积分数等于氧气的体积除以空气的总体积乘以百分子一般。该实验中水倒流入集气瓶中的体积则为氧气的体积,故氧气的体积为V1-V2,空气的体积为V1,故氧气的体积分数=![]() ×100%,正确。故选C。
×100%,正确。故选C。

 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案【题目】学校化学兴趣小组的同学知道二氧化锰能作过氧化氢(H2O2)分解的催化剂后,想再探究其他一些物质如氧化铝是否也可作过氧化氢分解的催化剂。请你一起参与他们的探究过程,并填写下列空白.
【提出问题】氧化铝能不能作过氧化氢分解的催化剂呢?
【作出猜想】氧化铝能作过氧化氢分解的催化剂.
【实验验证】
实验步骤 | 实验现象 | 实验结论 | |
实验一 | _______________ | 有少量气泡 木条不复燃 | 常温下过氧化氢溶液分解速率很慢. |
实验二 | 在装有过氧化氢溶液的试管中加入少量氧化铝,然后将带火星的木条伸入试管中 | ________ | 氧化铝能加快过氧化氢的分解速率 |
【得出结论】氧化铝能加快过氧化氢的分解速率,故氧化铝能作过氧化氢分解的催化剂.
【反思提高】经过讨论,有的同学认为只有上述两个证据,不能证明氧化铝能作过氧化氢分解的催化剂,还要补充一个探究实验:
实验三:
【实验目的】探究_______________________________________ 。
【实验步骤】①准确称量氧化铝(少量)的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行__________,洗涤,干燥,称量;④对比反应前后氧化铝的质量.
【交流讨论】如果氧化铝在反应前后质量不变,则说明氧化铝可以作过氧化氢分解的催化剂.
【提出新的问题】但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验:探究_____________________________________ 。
【拓展探究】设计如下四组实验,比较二氧化锰和氧化铝对过氧化氢溶液分解的催化作用,其中观察效果最差的_________
|
|
|
|
第一组 | 第二组 | 第三组 | 第四组 |
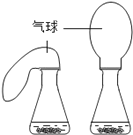
A.第一组同时实验,观察比较反应过程中两个气球体积的变化
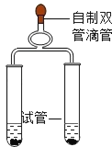
B.第二组同时实验,观察比较反应过程中两个试管内产生气泡的快慢
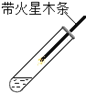
C.第三组分两次实验,看木条是否能复燃
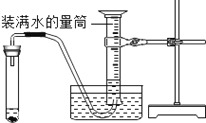
D.第四组分两次实验,比较收集一定体积的气体所需要的时间
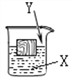
【题目】如下图,一木块漂浮于X中,向X中缓缓加入(或通入)少量物质Y后最终木块上浮,则X与Y可能是(溶液的体积变化忽略不计)( )
序号 | X | Y |
① | 水 | 食盐 |
② | 氢氧化钙溶液 | 二氧化碳 |
③ | 稀硫酸 | 镁粉 |
④ | 硫酸铜溶液 | 铁粉 |
A. ②④ B. ①③ C. ①②③ D. ②③④