题目内容
使铁和铜的混合物 20 g与足量的稀硫酸反应,可制得氢气0.4 g,求原混合物中铁和铜各为多少克?
8.8g
这是中考常见的一种题型。虽然题中给出的其中一个量是混合物的质量,但在初中阶段的化学计算,通常是只有一种物质能发生反应。所以只要能准确判断出究竟是哪种物质发生反应,就可按上题同样的方法进行解答了。本题中的铁和铜根据金属活动顺序可知,铜不能置换出氢气,所以应根据铁与酸的反应来计算。
解:设原混合物中含铁的质量为x
Fe+H2SO4 = FeSO4+ H2↑
56 2
x 0.4g
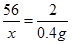
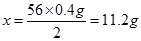
则混合物中铜的质量即为:20g-11.2g=8.8g
解:设原混合物中含铁的质量为x
Fe+H2SO4 = FeSO4+ H2↑
56 2
x 0.4g
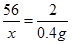
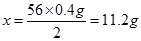
则混合物中铜的质量即为:20g-11.2g=8.8g

练习册系列答案
相关题目