题目内容
【题目】实验是科学探究的重要途径,请回答下列有关化学实验的问题。
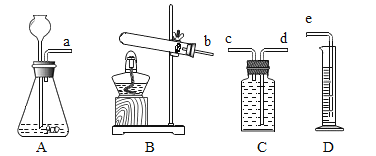
(1)在实验桌上有如下几种气体发生装置和收集装置。请你参与实验并回答问题:
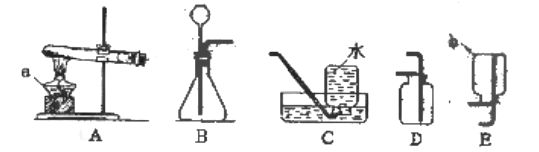
实验室用石灰石与稀盐酸反应制取并收集二氧化碳,应选择的装置为_______(填字母)。制取CO2的化学方程式为________,组装气体发生装置后,应先检查装置的_____________,再添加药品。
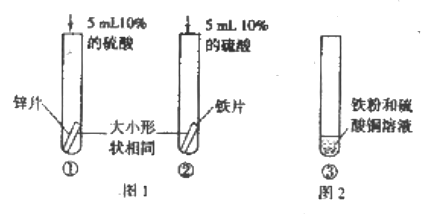
(2)在探究Zn、Fe、Cu三种金属的有关性质时,进行了如图所示的实验,通过以上三个实验,___________(填“能”或“不能”)得出Zn、Fe、Cu三种金属的活动性顺序。实验结束后,将图1中剩余的两种金属片放入图2试管③中,充分反应后试管③中的溶液为无色,则试管③中的固体一定含有___________。
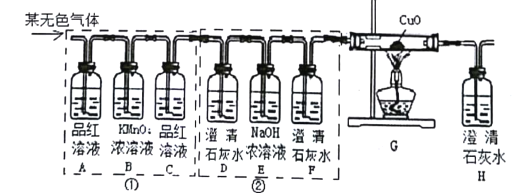
(3)某化学兴趣小组的同学利用如图微型实验装置进行探究实验。
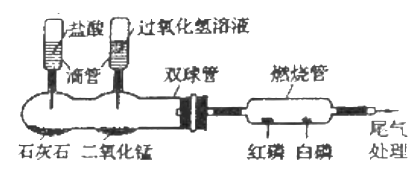
①挤压右滴管并微热燃烧管,白磷燃烧而红磷不燃烧,由此可说明燃烧需要什么条件__________?
②相同质量的磷、铁、镁分别在氧气中完全燃烧,消耗氧气最多的是____________。
(4)一同学用某铁合金样品做了如下实验:称量11.4g样品,放入质量为40g的烧杯中,再往烧杯中加入200g稀硫酸,恰好完全反应(杂质不与酸反应,也不溶于水)。反应完毕后称量,烧杯及烧杯内物质总质量为251g。求所用稀硫酸的溶质质量分数__________。
【答案】BD CaCO3+2HCl=CaCl2+H2O+CO2↑ 气密性 能 铁、铜(或Fe、Cu) 温度达到可燃物的着火点 磷 9.8%
【解析】
(1)实验室用石灰石固体与稀盐酸反应制二氧化碳,反应物是固液混合,反应条件是常温,发生装置选B,二氧化碳可溶于水且与水反应,密度比空气大且与空气中各成分不反应,收集装置应选D,制取装置故填BD;石灰石和稀盐酸反应生成二氧化碳、氯化钙和水,化学方程式故填CaCO3+2HCl=CaCl2+H2O+CO2↑;组装气体发生装置后,应先检查装置的气密性,然后再添加药品,故填气密性;
(2)图1实验锌表面产生气泡的速率比铁快,能证明锌比铁活泼,图2实验铁粉表面有红色物质生成,证明铁比铜活泼,通过以上三个实验,能得出Zn、Fe、Cu三种金属的活动性顺序,故填能;实验结束后,将图1中剩余的两种金属片放入图2试管③中,充分反应后试管③中的溶液为无色,说明溶液中的铜离子和亚铁离子都被置换出来了,说明试管③中的固体一定含有铁和铜,故填铁、铜(或Fe、Cu);
(3)
①挤压右滴管使过氧化氢溶液被二氧化锰催化生成氧气,微热燃烧管是温度升高,白磷燃烧而红磷不燃烧,由此可说明燃烧需要温度达到可燃物的着火点,故填温度达到可燃物的着火点;
②根据磷、铁、镁燃烧的化学方程式可知,假设质量为m的磷、铁、镁分别在氧气中完全燃烧,



可知消耗氧气的质量大小为![]() >
>![]() >
>![]() ,消耗氧气最多的故填磷;
,消耗氧气最多的故填磷;
(4)由题意可知,铁和稀硫酸反应生成硫酸亚铁和氢气,反应的方程式为Fe+H2SO4═FeSO4+H2↑,根据质量守恒定律可知生成氢气的质量=11.4g+40g+200g-251g=0.4g,设所用稀硫酸的溶质质量分数为x,x

解得x=9.8%,故填9.8%。

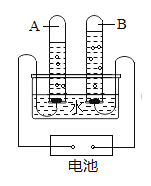
【题目】学习了金属的性质后,同学们设计了以下实验验证铁铜银的金属活动性顺序
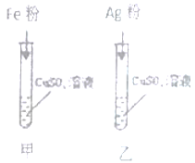
(1)能证明铁铜银活动性顺序的现象是________。
(2)甲试管内的化学反应方程式为________。
(3)实验结束后,将甲乙试管内的剩余物质都倒在一起,充分反应过滤,得到滤渣和滤液。
探究一、A组同学对滤渣的成分进行探究,向滤渣中加入稀盐酸,观察到无气泡产生,滤渣的成分为_______。
探究二、B组同学对滤液成分进行探究,提出猜想
猜想一:溶质只有FeSO4猜想二:_________
设计实验
实验步骤 | 实验现象 | 结论 |
取一定量滤液于试管中,____ | ________ | 猜想二正确 |
【题目】为研究锌和铝的金属活动性 ,某研究小组进行了如下探究。
(1)小明设计方案:向表面积相同的铝片和锌粒中分别加入盐酸,根据反应的快慢判断两者的活动性强弱。写出铝与盐酸反应的化学方程式:________。
(2)小芳将一砂纸打磨过的铝片放入一定量的盐酸中,发现有气泡产生 ,还观察到有“灰黑色沉淀”这一异常现象出现。
(提出问题)铝与盐酸反应出现的灰黑色沉淀的组成是什么?
(查阅文献)①铝在颗粒较小时为灰黑色,AlCl3为无色透明晶体或白色而微带浅黄色的固体,易溶于水和乙醇。②一种金属加入到两种活动性均比它弱的金属化合物溶液的混合液中,会先置出最弱的金属。再置换出第二种金属。该金属会先和最弱的金属盐溶液反应。
(提出合理假设)假设a:该灰黑色沉淀可能含有_________;假设b:该灰黑色沉淀可能含有AlCl3;假设c:该灰黑色沉淀可能含有难溶于酸的物质。
(设计并完成实验)取灰黑色沉淀分别进行如下实验。
实验编号 | 实验操作 | 实验现象 |
① | 加入适量稀盐酸 | 有微量气泡,固体全部溶解,得到澄清溶液 |
② | 加入适量蒸馏水 | 固体部分溶解 |
③ | 加入适量无水乙醇 | 固体部分溶解 |
(得出结论)由实验①可判断假设c_____________(填“成立”或“不成立”,)再集合②和③可得出该灰黑色沉淀的成分是__________。
(3)你认为①中小明的实验能否比较锌和铝的金属活动性强弱?______(填“能”或“不能”),分别从设计方法或操作可行性的角度,具体说明理由(一点即可)_____。
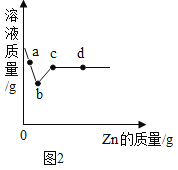
(拓展延伸)附加分:若正确回答下列小题,将获得4分的奖励 ,但化学试卷总分不超过60分。为继续研究另一种金属锌的化学性质,小敏向一定质量的硝酸银和硝酸铜的混合溶液中加入锌粉,溶液质量与加入锌的质量关系如图所示。那么,在a点时,溶液里含的金属化合物有_________种;bc段发生的化学反应方程式为_________;d点得到的固体的成分为_____