题目内容
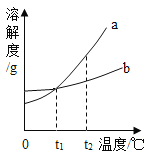
【题目】如图是a、b、e三种固体物质的溶解度曲线,下列说法错误的是( )
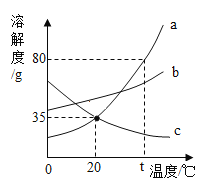
A.t℃时,将等质量的a、b、c加水配成饱和溶液,所得溶液质量的大小关系是:c>b>a,
B.t℃时,45g a的饱和溶液要稀释为40%的溶液需要加水5g
C.a中含有少量b,可用冷却a的热饱和溶液的方法提纯a
D.将20℃时的三种物质的饱和溶液升温到t℃,所得溶液中溶质的质量分数的大小关系是:b>a=c
【答案】D
【解析】
A、t℃时,a物质的溶解度最大,c物质的溶解度最小,所以溶解等质量的a、b、c三种固体配制成t℃时的饱和溶液,所得溶液质量的大小关系是:c溶液>b溶液>a溶液,故正确;
B、t℃时,45g a的饱和溶液中含有a的质量为45g![]()
![]() =20g,稀释为40%的溶液质量为20g
=20g,稀释为40%的溶液质量为20g![]() 40%=50g,需要水的质量为50g-45g=5g,故正确;
40%=50g,需要水的质量为50g-45g=5g,故正确;
C、a中含有少量b,可用冷却a的热饱和溶液的方法提纯a正确,故正确;
D、将20℃时三种物质的饱和溶液升温到t℃时,a、b物质的溶解度增大且在20℃时b>a,c物质的溶解度减小,析出晶体,所以所得溶液M中溶质的质量分数的大小关系是:b>a>c,故错误;
故选D。

 学业测评一课一测系列答案
学业测评一课一测系列答案【题目】请回答下列问题:
(1)铝热反应是焊接铁路上钢轨的反应原理:即在高温下铝与氧化铁发生反应生成氧化铝和铁,写出该反应的化学方程式_____该反应属于_____反应(填基本类型)
(2)下面是部分金属的部分物理性质:
物理性质 | 物理性质比较 |
导电性 |
|
密度 |
|
由上表可知:用铝作高空电缆是因为_____、_____。
(3)认真观察分析比较下列几个反应及现象:
A “真金不怕火炼”金在高温下也不与氧气发生反应。Au+O2![]() (不反应)
(不反应)
B 金属镁在空气中燃烧,发出耀眼的强光,放出大量的热量。2Mg+O2![]() 2MgO
2MgO
C 铜在加热条件下与氧气发生反应,在表面变黑。2Cu+O2![]() 2CuO
2CuO
D 铝在空气中与氧气发生反应,在表面生成一层致密的氧化膜。2Al+3O2=2Al2O3
从上述实验事实可以看出,四种金属的活动性顺序是_____。