题目内容
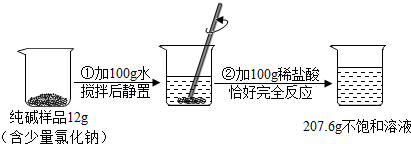
实验室用过氧化氢溶液与二氧化锰混合制氧气,反应结束,共收集到559mL气体.实验测得相关数据如下图所示:(结果保留1位小数)
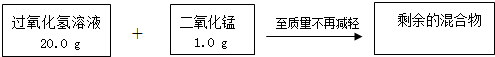
(1)反应结束后,过滤,滤渣的质量为 g.
(2)反应产生氧气的质量为 g.(标准状况下氧气的密度约为1.43g/L)
(3)过氧化氢溶液中溶质的质量分数(百分数).

(1)反应结束后,过滤,滤渣的质量为
(2)反应产生氧气的质量为
(3)过氧化氢溶液中溶质的质量分数(百分数).
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)二氧化锰是过氧化氢分解的催化剂,催化剂在化学反应前后质量不变;
(2)根据密度公式可以求出氧气的质量;
(3)根据过氧化氢分解的化学方程式和(1)中计算出的氧气的质量,就可计算出参与反应的过氧化氢的质量,然后根据质量分数公式计算即可.
(2)根据密度公式可以求出氧气的质量;
(3)根据过氧化氢分解的化学方程式和(1)中计算出的氧气的质量,就可计算出参与反应的过氧化氢的质量,然后根据质量分数公式计算即可.
解答:解:
(1)因为催化剂在化学反应前后质量不变,故混合物中二氧化锰的质量为1.0g;
(2)559mL=0.559L,反应产生氧气的质量为0.559L×1.43g/L=0.8g;
(3)设过氧化氢溶液中溶质的质量为x.
2H2O2
2H2O+O2↑
68 32
x 0.8g
=
x=1.7g
过氧化氢溶液中溶质的质量分数
×100%=8.5%
答案:
(1)1.0
(2)0.8
(3)过氧化氢溶液中溶质的质量分数8.5%
(1)因为催化剂在化学反应前后质量不变,故混合物中二氧化锰的质量为1.0g;
(2)559mL=0.559L,反应产生氧气的质量为0.559L×1.43g/L=0.8g;
(3)设过氧化氢溶液中溶质的质量为x.
2H2O2
| ||
68 32
x 0.8g
| 68 |
| 32 |
| x |
| 0.8g |
x=1.7g
过氧化氢溶液中溶质的质量分数
| 1.7g |
| 20g |
答案:
(1)1.0
(2)0.8
(3)过氧化氢溶液中溶质的质量分数8.5%
点评:要想解答好这类题目,首先,要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等.然后,根据所给的问题情景等,结合所学的相关知识和技能,细致地分析题意等各种信息资源,按照题目要求进行认真地选择或解答即可.

练习册系列答案
相关题目
我省环保部门按新修订的《环境空气质量标准》,着力做好细颗粒物(PM2.5)和臭氧(O3)等新增指标的监测.下列说法正确的是( )
| A、燃烧植物秸秆不会造成大气污染 |
| B、吸入细颗粒物对人体健康没有危害 |
| C、化学在环境监测和保护中起重要作用 |
| D、臭氧和氧气都是由同一种微粒构成 |
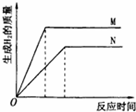 等质量的M、N两种金属,分别与相同质量分数的足量的稀盐酸反应(已知M、N在生成生物中均为+2价),生成的氢气的质量和反映的时间如图所示.由图中的两条曲线,可以得哪些结论.(答两条)
等质量的M、N两种金属,分别与相同质量分数的足量的稀盐酸反应(已知M、N在生成生物中均为+2价),生成的氢气的质量和反映的时间如图所示.由图中的两条曲线,可以得哪些结论.(答两条)