题目内容
为测定某纯碱样品(含少量氯化钠杂质)中碳酸钠的含量,进行了如图所示的实验操作,试根据实验过程和提供的数据(步骤②产生的气体全部逸出)回答下列问题: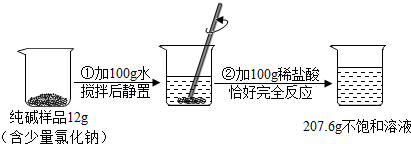
(1)反应生成二氧化碳的质量为 g
(2)12g样品中碳酸钠的质量为 g
(3)稀盐酸中溶质的质量分数(写出计算过程).

(1)反应生成二氧化碳的质量为
(2)12g样品中碳酸钠的质量为
(3)稀盐酸中溶质的质量分数(写出计算过程).
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:反应前后的质量差即为反应生成二氧化碳的质量;
根据二氧化碳的质量可以计算碳酸钠的质量和稀盐酸中氯化氢的质量,进一步可以计算稀盐酸中溶质的质量分数.
根据二氧化碳的质量可以计算碳酸钠的质量和稀盐酸中氯化氢的质量,进一步可以计算稀盐酸中溶质的质量分数.
解答:解:(1)反应生成二氧化碳的质量为:12g+100g+100g-207.6g=4.4g,
故填:4.4.
(2)设碳酸钠的质量为x,氯化氢的质量为y,
Na2CO3+2HCl═2NaCl+H2O+CO2↑,
106 73 44
x y 4.4g
=
=
,
x=10.6g,y=7.3g,
答:12g样品中碳酸钠的质量为10.6g.
(3)稀盐酸中溶质的质量分数为:
×100%=7.3%,
答:稀盐酸中溶质的质量分数为7.3%.
故填:4.4.
(2)设碳酸钠的质量为x,氯化氢的质量为y,
Na2CO3+2HCl═2NaCl+H2O+CO2↑,
106 73 44
x y 4.4g
| 106 |
| x |
| 73 |
| y |
| 44 |
| 4.4g |
x=10.6g,y=7.3g,
答:12g样品中碳酸钠的质量为10.6g.
(3)稀盐酸中溶质的质量分数为:
| 7.3g |
| 100g |
答:稀盐酸中溶质的质量分数为7.3%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
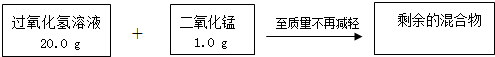
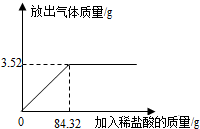 为测定石灰石样品中碳酸钙的质量分数,某学习小组进行了如下实验探究,取10g石灰石样品放入烧杯中,加入稀盐酸至不再产生气泡为止(石灰石中的杂质不溶于水,也不反应),并绘制了加入稀盐酸的质量与放出气体质量的坐标图,见图.
为测定石灰石样品中碳酸钙的质量分数,某学习小组进行了如下实验探究,取10g石灰石样品放入烧杯中,加入稀盐酸至不再产生气泡为止(石灰石中的杂质不溶于水,也不反应),并绘制了加入稀盐酸的质量与放出气体质量的坐标图,见图. 小明和小丽从新闻媒体得知,今年春季,西南5省面临世纪大旱,群众饮水极度困难,甚至一些浊水都已经成为生命之源.两同学决定对此开展探究,与西南群众生命健康献上自己的一份心意.请你参与他们的研究,并完成相关问题:
小明和小丽从新闻媒体得知,今年春季,西南5省面临世纪大旱,群众饮水极度困难,甚至一些浊水都已经成为生命之源.两同学决定对此开展探究,与西南群众生命健康献上自己的一份心意.请你参与他们的研究,并完成相关问题: