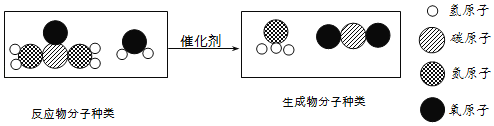
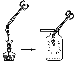
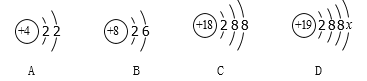
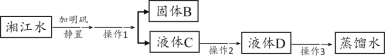��Ŀ����
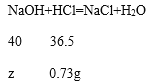
����Ŀ��ijУ���꼶�����ǰ���ѧ���С���ͬѧ����̽����Ļ�ѧ����ʱ���������ͼ��ʾ��A��B����ʵ�顣����ش��������⣺
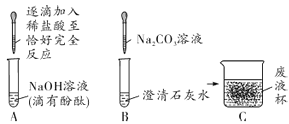
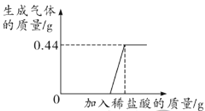
��1��Aʵ���з�̪��������_______���������Ļ�ѧ��Ӧ����ʽΪ___________��
��2��Bʵ���пɹ۲쵽��������__________��
��3��ʵ�����֧�Թ��еķ�Һ�������Һ��C�У����ֻ�Ϸ�Һ���Dz��Ժ�ɫ��
������˼����ͬѧ�Ǿ���˼��һ����Ϊ����Ϸ�Һ�Ժ�ɫ��Bʵ����Թ��е�������Aʵ����Թ��еķ�̪��Ӧ�Ľ����
��������⣩Bʵ����Թ��е�������ʲô��
���������룩����һ���Թ��е�������NaOH����������Թ��е�������____________��
���������Թ��е�������Ca(OH)2��NaOH��
��ʵ����֤����ѩͬѧ���÷�Һ��C�еĻ�Ϸ�Һ��ȷ��Bʵ����Թ��е����ʣ���һ�������ķ�Һ���ˣ�ȡ10g��Һ����������μ�����������Ϊ7.3% ��ϡ���ᣬ������ϡ���������Ϊ20gʱ��Ӧ��ȫ����������ϡ���ᣬ����������������ӣ����ݷ�Ӧ����õ���ͼ��ʾ��ͼ��
���������ϣ�̼������Һ��ϡ����ķ�Ӧ�Ƿֲ����еġ�������̼������ϡ���ᷴӦ����̼�����ƺ��Ȼ��ƣ�Na2CO3 + HCl===NaHCO3 +NaCl��Ȼ�������ɵ�̼��������ϡ���ᷴӦ�����Ȼ��ơ�������̼�����ˮ��NaHCO3+HCl===NaCl+CO2��+H2O��
��ʵ����ۣ����Խ��ۣ�����ͼ��ó������������ȷ�ģ�������������________���ѧʽ��������һ�Ͳ������Ǵ���ģ�ԭ����_______��
�������ۣ�10g��Һ�к���______g NaOH��_______g Na2CO3��_______g Ca(OH)2��
����չ���������������һ��ʵ�飬����֤���������������ȷ�ģ�_________��
���𰸡��ж�����Ƿ�ǡ����ȫ��Ӧ NaOH+HCl=NaCl+H2O ����ʯ��ˮ����� Na2CO3��NaOH CO2 ϡ�����Ca(OH)2��NaOH��Ӧ�������������� 0.8 1.06 0 ���Һ��C�еĻ�Ϸ�Һ�м�������ϡ���ᣬ�������ݲ�����֤�������������ȷ
��������
��1��������ǡ�ú�����������Һ��Ӧʱ�����з�̪������������Һ��Ϊ��ɫ������Aʵ���з�̪���������ж�����Ƿ�ǡ����ȫ��Ӧ��ϡ������������Ʒ����кͷ�Ӧ�����Ȼ��ƺ�ˮ����Ӧ����ʽΪ��NaOH+HCl=NaCl+H2O��Bʵ����̼���ƺ��������Ʒ�����Ӧ����̼��ƺ�ˮ�����Կ�����ʵ�������dz���ʯ��ˮ����ǣ�
����������Bʵ����Թ��е����ʷ�Ϊ���������̼������Һ������������Һǡ����ȫ��Ӧ��������NaOH��̼������ʣ������������Na2CO3��NaOH������������Һ��ʣ����������Ca(OH)2��NaOH�����Բ�������Թ��е�������Na2CO3��NaOH��
ʵ���������������ͷ���ͼ���Լ��������ϣ�̼������Һ��ϡ����ķ�Ӧ�Ƿֲ����еġ�������̼������ϡ���ᷴӦ����̼�����ƺ��Ȼ��ƣ�Na2CO3 + HCl===NaHCO3 +NaCl��Ȼ�������ɵ�̼��������ϡ���ᷴӦ�����Ȼ��ơ�������̼�����ˮ��NaHCO3+HCl===NaCl+CO2��+H2O���������Ὺʼû�ж�����̼��������Ӧ�������ж�����̼���������Բ��������ȷ�ģ�������������CO2��ϡ�����Ca(OH)2��NaOH��Ӧ�������������ɣ����Բ���һ�Ͳ������Ǵ���ģ�
���ݲ������Ͽ�֪��Na2CO3 �� HCl��Ӧ�����������Ȼ��ơ�ˮ�Ͷ�����̼����Ӧ�Ļ�ѧ����ʽ��Na2CO3+2HCl=NaCl+CO2��+H2O����������μӷ�Ӧ��HCl����=20g��7.3%=1.46g������Na2CO3+2HCl=NaCl+CO2��+H2O�ķ�Ӧ��Na2CO3������Ϊx�����ĵ�HCl��y��NaOH+HCl=NaCl+H2O�ķ�Ӧ��NaOH������Ϊz����
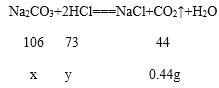
![]() x=1.06g
x=1.06g
![]() y=0.73g
y=0.73g
NaOH+HCl=NaCl+H2O�ķ�Ӧ��HCl������Ϊ��1.46��0.73=0.73g��
![]() z=0.8g��������Һ�д���̼���ƣ�̼�������������Ʒ�Ӧ����̼��Ƴ������������ƣ���Һ�����ܴ����������ƣ��������Ƶ�����Ϊ0g��10g��Һ�к���0.8g NaOH��1.06g Na2CO3��0g Ca(OH)2��
z=0.8g��������Һ�д���̼���ƣ�̼�������������Ʒ�Ӧ����̼��Ƴ������������ƣ���Һ�����ܴ����������ƣ��������Ƶ�����Ϊ0g��10g��Һ�к���0.8g NaOH��1.06g Na2CO3��0g Ca(OH)2��
��չ���������������ȷ��ֻҪ֤����Һ�е����ʴ���̼���ƣ�̼��������ϡ���ᷴӦ���������ơ�ˮ�Ͷ�����̼�����Һ��C�еĻ�Ϸ�Һ�м���������ϡ���ᣬ�������ݲ�����֤�������������ȷ��

����Ŀ��ij��ѧ������ʦָ����̽������ˮ�����ķ�Ӧ��
(1)��ͼ��װ��ҩƷ������װ��(�г���������ȥ)������Aװ�õ�������________��
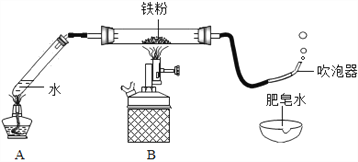
(2)����һ��ʱ���ɫ������ڣ������������������ݣ����������Ϸ�����ȼ�ŵ�ľ���������ݣ��ܲ���������������ȼ�յĻ�ѧ����ʽΪ_____________��
(3)ͬѧ�����ۺ���Ϊ������ˮ������Ӧ���ɵĹ�����������һ�������������������ڵĺ�ɫ�����л����ܺ�����������������
���������ϡ���������������(FeO��Fe2O3��Fe3O4)������FeO�Ӵ��������������ɺ�ɫ��Ϊ����ɫ���������������ﶼ��������ͭ��Һ��Ӧ��
��ʵ��̽����
ʵ�鲽�� | ʵ������ | ʵ����� |
�����������к�ɫ���壬ƽ���ڰ�ֽ�� | ��ɫ���岻��ɫ | ��ɫ������һ��û��____(����������) |
ȡ������ɫ����������װ���Թܣ���������____��Һ | ________�����к�ɫ������� | ��ɫ������һ������__________ѧ�ƣ��� |
��̽�����ۡ�����ˮ���������û���Ӧ���йصĻ�ѧ����ʽ��_________��
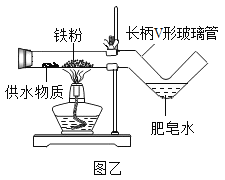
����չ���¡�ͬѧ������������������V�β��������Ľ���ͼ��װ�ã���Ƴ�ͼ��װ�ã����ֱ�ѡ��ʪ����ʪ�۱ʡ�«��Ҷ���Ž�����������þ��������ͭ����Ϊ��ˮ����ʵ�鶼��óɹ���
�ټס���װ����ȣ���װ���кܶ��ŵ㣬����д��һ����__________��
�ڷ���������ˮ���Ĺ�ˮԭ����������ȷ����______(����ĸ)
A�����ɡ�������ʣ������õ���ˮ�ͱ�ˮ����
B�����ʵĸ�ˮֲ�������ʱˮ�������ͷų���
C����������ˮ�Ĺ������ʣ�����������ˮ��
����Ŀ��ijͬѧΪ�˲ⶨʵ�������������Ʒ�Ĵ��ȡ�ȡ2.5�˸���Ʒ��0.5�˶������̻�ϣ�����һ��ʱ������ʲ��μӷ�Ӧ������ȴ������ʣ�����������ظ�������������¼�������±���
����ʱ�� | T1 | T2 | T3 | T4 |
ʣ�������� | 2.12 | 2.08 | 2.04 | 2.04 |
�ټ��ȵ�T2ʱ���������Ƿ��Ѿ���Ӧ��ȫ��_____
����Ʒ������ص���������_______