��Ŀ����
����Ŀ����������װ�ã������ѧ֪ʶ�ش����⡣
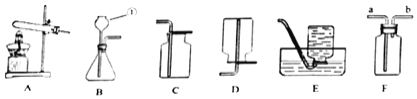
![]() ��������ٵ�������______��
��������ٵ�������______��
![]() ����������______����ʹ��Fװ���ռ�����������Ӧ�ô�______�ڽ���
����������______����ʹ��Fװ���ռ�����������Ӧ�ô�______�ڽ���![]() �a����b��
�a����b��![]() ��
��
![]() ʵ����ѡ��װ��B��C��ȡ������̼����Ӧ�Ļ�ѧ����ʽ�ǣ�______�������ķ�����______�������ռ�������ͨ����ɫʯ����Һ�У�������������______��
ʵ����ѡ��װ��B��C��ȡ������̼����Ӧ�Ļ�ѧ����ʽ�ǣ�______�������ķ�����______�������ռ�������ͨ����ɫʯ����Һ�У�������������______��
![]() �����н���������Ȼ��ȡů����Ȼ������Ҫ�ɷ��Ǽ��飬ijͬѧͨ���������ϣ�֪��ʵ�������ˮ�����ƹ�������ʯ�Ҽ�����ȡ���飬ͨ������¼�����ܶȱȿ���С��������ˮ��ʵ������ȡ����ѡ��ķ���װ����______
�����н���������Ȼ��ȡů����Ȼ������Ҫ�ɷ��Ǽ��飬ijͬѧͨ���������ϣ�֪��ʵ�������ˮ�����ƹ�������ʯ�Ҽ�����ȡ���飬ͨ������¼�����ܶȱȿ���С��������ˮ��ʵ������ȡ����ѡ��ķ���װ����______![]() ����ĸ
����ĸ![]() �����ռ�����ļ��������ѡ��______װ��
�����ռ�����ļ��������ѡ��______װ��![]() ��
��![]() ��ѡ��
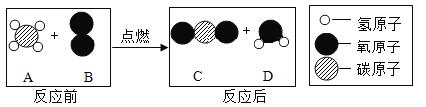
��ѡ��![]() �������ʹ����Ч�ظ����˿���������������ȫȼ�յĻ�ѧ����ʽ��______��
�������ʹ����Ч�ظ����˿���������������ȫȼ�յĻ�ѧ����ʽ��______��
���𰸡�����©�� ��ɫ��ĩ״���� a ![]() ��һ��ȼ�ŵ�ľ��ƽ���ڼ���ƿ�ڣ�ľ��Ϩ��֤������ ��ɫʯ����Һ��ɺ�ɫ A D
��һ��ȼ�ŵ�ľ��ƽ���ڼ���ƿ�ڣ�ľ��Ϩ��֤������ ��ɫʯ����Һ��ɺ�ɫ A D ![]()
��������
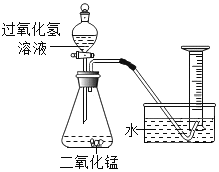
![]() �����ٵ������dz���©����
�����ٵ������dz���©����
![]() ���������Ǻ�ɫ��ĩ״���壻�������ܶȱȿ�����������װ��F�ռ�����ʱ�������ӳ��ܽ��룻
���������Ǻ�ɫ��ĩ״���壻�������ܶȱȿ�����������װ��F�ռ�����ʱ�������ӳ��ܽ��룻
![]() ʵ������ȡ������̼��ԭ����̼��������ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼����ѧ����ʽΪ��
ʵ������ȡ������̼��ԭ����̼��������ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼����ѧ����ʽΪ��![]() ��������̼��ȼ�ա�Ҳ��֧��ȼ�գ���������ʱ��ȼ�ŵ�ľ�����ڼ���ƿ�ڣ���ľ��Ϩ��֤������������������̼��ˮ��Ӧ����̼�ᣬ̼����ʹ��ɫ��ʯ����Һ���ɫ��
��������̼��ȼ�ա�Ҳ��֧��ȼ�գ���������ʱ��ȼ�ŵ�ľ�����ڼ���ƿ�ڣ���ľ��Ϩ��֤������������������̼��ˮ��Ӧ����̼�ᣬ̼����ʹ��ɫ��ʯ����Һ���ɫ��
![]() ʵ���ҿ�����ˮ�����ƹ�������ʯ�Ҽ�����ȡ���飬�����Ҫ���ȣ�ѡ��Aװ�ã�ͨ������¼�����ܶȱȿ���С��������ˮ����˼�������������ſ���������ˮ���ռ��������ſ������ռ��ļ���Ƚϸ������������ڵ�ȼ�����������ɶ�����̼��ˮ����Ӧ����ʽΪCH4+2O2
ʵ���ҿ�����ˮ�����ƹ�������ʯ�Ҽ�����ȡ���飬�����Ҫ���ȣ�ѡ��Aװ�ã�ͨ������¼�����ܶȱȿ���С��������ˮ����˼�������������ſ���������ˮ���ռ��������ſ������ռ��ļ���Ƚϸ������������ڵ�ȼ�����������ɶ�����̼��ˮ����Ӧ����ʽΪCH4+2O2![]() 2H2O+CO2��
2H2O+CO2��

����Ŀ�����������������������й㷺Ӧ�á�ʵ��С��Թ��������ijЩ���ʽ����о���
���ȶ���
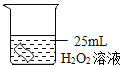
��1����ͼ��ʾ����ʵ�飬��������ֽ�Ļ�ѧ����ʽΪ______������3.2gO2ʱ�ֽ�Ĺ������������Ϊ______g��
��2��������ˮ���ռ�O2��ԭ����______��
��3��̽���¶ȶԹ�������ֽ����ʵ�Ӱ��
ͬѧ�ǽ��������µ�ʵ�飬ʵ���������±���
ʵ����� | �� | �� | �� |
H2O2��Һ��Ũ��% | 30 | 30 | 30 |
H2O2��Һ�����/mL | 6 | 6 | 6 |
�¶�/�� | 20 | 35 | 55 |
MnO2������/g | 0 | 0 | 0 |
�ռ�O2�����/mL | 0 | 1.9 | 7.8 |
��Ӧʱ�� | 40min | 40min | 40min |
�ɴ˵ó��Ľ�����______��
��ʴ��
���������ϣ�H2O2��Һ�и�ʴ�ԡ�
������ʵ�飩
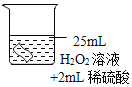
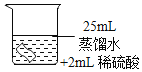
��ͭƬ�ֱ������3����Һ�н���ʵ�飬���±���
��� | �� | �� | �� |
ʵ�� |
|
|
|
һ��ʱ�������� | �����Ա仯 | ��Һ��������������ϸС���� | �����Ա仯 |
����������ۣ�
��4��ʵ��ٵ�������______��
��5��ͭƬ����ʴ�ķ�Ӧ���£���ȫ�÷�Ӧ�Ļ�ѧ����ʽ��Cu+H2O2+H2SO4=CuSO4+______��
����˼������
��6��ijͬѧ�����ʵ����У���������5���ķ�Ӧ�⡣��������һ����Ӧ������ϸС���ݲ������÷�Ӧ�ķ�Ӧ��Ϊ______��