题目内容
【题目】盛有等质量、等质量分数稀盐酸的两只烧杯,放在托盘天平的左右两盘,天平平衡,在左盘烧杯中加入10gCaCO3,恰好完全反应,若要使天平重新平衡,则右盘烧杯中应加入的下列物质是
A. 5.6g铁和锌B. 10g镁和氧化镁
C. 10g碳酸镁D. 10g碳酸钠和碳酸锌
【答案】C
【解析】
设:10g碳酸钙完全反应生成二氧化碳的质量为x。
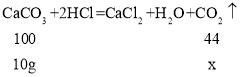
![]() x=4.4g;左盘增加的质量是10g-4.4g=5.6g。右边烧杯的质量增加量也为5.6g天平才能保持平衡。
x=4.4g;左盘增加的质量是10g-4.4g=5.6g。右边烧杯的质量增加量也为5.6g天平才能保持平衡。
A、假设该金属全部是铁,设生成氢气的质量是y。
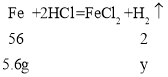
![]() y=0.2g;
y=0.2g;
假设该金属全部是锌,设生成氢气的质量是z。
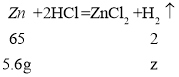
![]() z≈0.17g;所以5.6g铁和锌后,右盘中实际增加的质量在5.4g~5.43g之间,不管是铁、锌以何种比例混合右盘的增重不等于5.6g,故A错误;
z≈0.17g;所以5.6g铁和锌后,右盘中实际增加的质量在5.4g~5.43g之间,不管是铁、锌以何种比例混合右盘的增重不等于5.6g,故A错误;
B、假设该金属全部是锌,设生成氢气的质量是a。
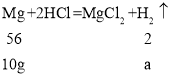
![]() a≈0.83g,由于氧化镁与盐酸反应生成氯化镁和水,所以不管是镁、氧化镁以何种比例混合右盘的增重一定大于5.6g,故B错误;
a≈0.83g,由于氧化镁与盐酸反应生成氯化镁和水,所以不管是镁、氧化镁以何种比例混合右盘的增重一定大于5.6g,故B错误;
C、根据化学方程式MgCO3+2HCl=MgCl2+CO2↑+H2O可知,每84份质量的碳酸镁与73份质量的盐酸反应,生成44份质量的二氧化碳,10克碳酸镁参加反应时盐酸不足,所以根据消耗7.3gHCl的质量计算生成二氧化碳的质量为4.4g,右边烧杯的质量增加量=10g-4.4g=5.6g,所以加入10克碳酸镁天平平衡,故C正确;
D、由于碳酸钙的相对分子质量是100,所以要想在加入10g碳酸盐的混合物生成的二氧化碳也是4.4g,必须是两种碳酸盐的相对分子质量一个大于100另一个小于100,碳酸钠的相对分子质量是106、碳酸锌的相对分子质量是125,所以加入10克碳酸钠和碳酸锌不可能使天平平衡,故D错误。故选C。

 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
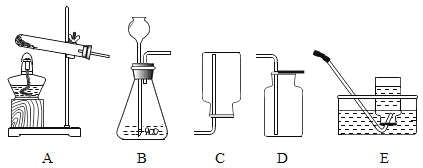
课课通课程标准思维方法与能力训练系列答案【题目】高阳同学通过阅读课外资料得知,潜水艇中常用过氧化钠(Na2O2)作为供氧剂,有关反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2,2Na2O2+2H2O═4NaOH+O2↑。于是她用如图所的装置来制取CO2并验证其与Na2O2的反应。
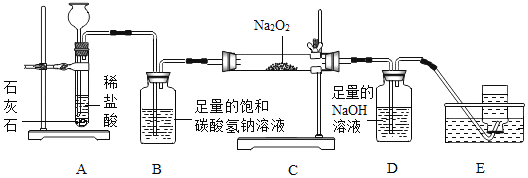
(1)装置B的作用是_____。
(2)反应一段时间后,装置E中收集到的气体主要是_____;反应后装置C硬质玻璃管中固体的成分是什么?高阳为此又进行了如下探究:
(猜想与假设)
猜想一 Na2CO3
猜想二Na2CO3和Na2O2
猜想三Na2CO3和NaOH
你认为还可能是_____
(设计实验)
实验操作 | 实验现象 | 实验结论 |
①取少量样品于试管中,加入足量的水,振荡 | 固体完全溶解,_____ | 样品中一定没有Na2O2 |
②取少量实验①所得溶液于另一试管中,加入过量的BaCl2溶液,振荡 | 有白色沉淀产生 | 猜想三正确 |
③取少量实验②所得上层清液于另一试管中,加入_____溶液,振荡 | 有白色沉淀产生 |
(反思与评价)反应后装置C硬质玻璃管中的固体含有NaOH,原因可能是_____。
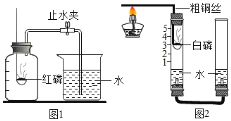
【题目】某化学兴趣小组的同学按照课本上的实验装置做“测定空气中氧气的体积分数”,实验(如图所示),但测出的氧气的体积分数明显小于1/5.
请你参与探究:
(提出问题)造成误差的原因是什么?如何改进课本上的实验装置?
(查阅资料)红磷、白磷的一些性质如下表:
颜色、状态 | 熔点/℃ | 着火点/℃ | 密度/(g/cm3) | |
红磷 | 暗红色固体 | 590 | 240 | 2.34 |
白磷 | 白色或黄色固体 | 44.1 | 40 | 1.82 |
(猜想与假设)
甲同学:可能是导管内原含有空气,后来留有吸入的水,影响实验的准确性。
乙同学:可能是瓶内残留气体中还有氧气。
你还能作出的猜想是____________.
(交流与讨论)
(1)丙同学认为用木炭代替红磷,就可以消除误差,大家认为他的猜想不合理,理由是___.
(2)他们对课本上的实验装置进行了如图所示的改进(其他仪器忽略).
①甲同学提出应把红磷换为白磷,则白磷燃烧的现象_________.(与红磷相同)
②与课本上的实验装置相比较,该装置的一个优点是____________.
③通过粗铜丝来点燃玻璃管内的白磷,这是利用了金属的_________性。
【题目】溶液在生产、生活中起着十分重要的作用。请回答下列问题:
(1)可以作为溶质的是___________。
A 只有固体 B 只有液体
C 只有气体 D 气体、液体、固体都可以
(2)配制100g质量分数为16%的氯化钠溶液,所需氯化钠的质量为___________,水的体积为_________mL (水的密度近似看作lg/cm3)。
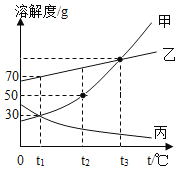
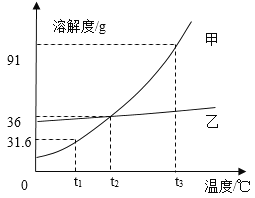
(3)甲、乙两种不含结晶水的固体物质的溶解度曲线如下图.t1℃时,甲物质的溶解度是___________。t2℃时,若从甲和乙两种物质的饱和溶液中析出等质量的固体,须蒸发掉较多水的是___________ (填“甲”或“乙”)物质的饱和溶液。
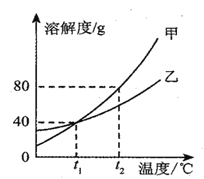
(4)下列说法正确的是___________。
A.将甲物质的饱和溶液变为不饱和溶液,其溶质的质量分数一定减小
B.将t2℃时甲、乙物质的溶液降温到t1℃,其溶液的质量一定相等
C.配制一定溶质质量分数的乙物质溶液,若量取水时俯视读数,其它操作均正确,则配制的乙溶液中溶质的质量分数将偏高
选项 | x | y |
A | 水 | 氧化钙 |
B | 水 | 硝酸铵 |
C | 浓硫酸 | 水 |
D | 稀盐酸 | 镁 |
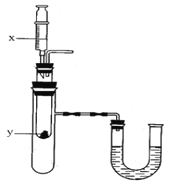
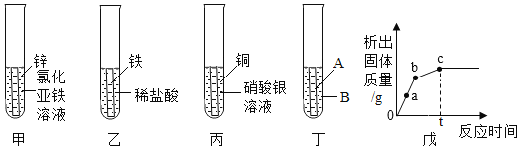
(5)按上图所示装置,将液体X注入装有固体y的试管中,会导致U形管中右端液面升高。则可能的组合是______________________。