题目内容
【题目】实验室收集到一桶含有FeSO4、CuSO4的废液,他们想从中回收金属铜和硫酸亚铁晶体,设计了如下实验方案。结合实验方案回答下列问题:
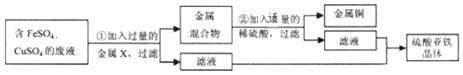
(1)步骤①中,金属X是_____。
(2)写出步骤①中反应的化学方程式_____。
(3)步骤①和②中涉及到的化学反应的基本反应类型为_____。
(4)在步骤②中,还能将金属混合物分离开的物理方法是_____。
【答案】Fe Fe+CuSO4=FeSO4+Cu 置换反应 用磁铁吸引
【解析】
(1)(2)由于目的是获得铜单质和硫酸亚铁,所以需要将铜离子转化为铜单质,而溶液中需要的是硫酸亚铁而不能引入新的杂质,所以加入的能够将铜离子转化为铜单质的只能是单质铁;据此写出反应的化学方程式;
(3)根据反应的特点分析反应的类型;
(4)根据铁能被磁铁吸引的特性分析。
(1)由题意可知,由于需要将铜离子转化为铜单质,而溶液还必须为硫酸亚铁,即不能引入新的杂质,所以可以加入铁将铜离子转化为铜单质;
(2)步骤①反应的化学方程式为:Fe+CuSO4=FeSO4+Cu;为保证CuSO4完全反应,Fe要过量;
(3)以上①②两反应中都是一种单质与一种化合物反应生成了另一种单质和另一种化合物,都属于置换反应;
(4)在步骤②中,还能将金属混合物分离开的物理方法是用磁铁吸引。

 名校课堂系列答案
名校课堂系列答案【题目】某化学兴趣小组为测定一批石灰石样品中碳酸钙的质量分数,取10g石灰石样品,把40g稀盐酸分4次加入样品中(样品中的其它成分既不与盐酸反应,也不溶于水),充分反应后经过滤、干燥、称量等操作,实验数据如下表:
实验 | 第一次 | 第二次 | 第三次 | 第四次 |
稀盐酸的用量 | 10g | 10 g | 10 g | 10 g |
剩余固体的质量 | X g | 4 g | 2 g | 2 g |
(1)表中X的值 为________g;
(2)该石灰石样品中碳酸钙的质量分数为_______;
(3)计算实验过程中产生二氧化碳气体的质量_______。(写出计算过程)
【题目】氯化钠的部分溶解度如下:
温度(℃) | 10℃ | 20℃ | 30℃ | 40℃ | 60℃ | 80℃ | 100℃ |
溶解度(g/100g水) | 35.8 | 36.0 | 36.1 | 36.4 | 37.1 | 38.0 | 39.2 |
①80℃氯化钠的溶解度是____g/100g水。
②20℃时,15g水中溶解____g氯化钠刚好形成饱和溶液。
③粗盐(含有泥沙的氯化钠)提纯的实验过程如图一所示,溶液A是____溶液(选填“饱和”或“不饱和”);操作Ⅱ是____。
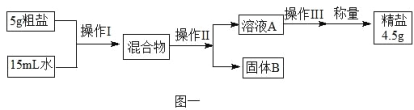
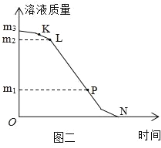
④操作Ⅲ过程中溶液质量与时间变化关系示意图如图二所示,相关分析正确的是___(选填编号)
a.m320g
b.L、P表示的溶液,溶质质量分数相同
c.m2m1是减少的水的质量
d.N点时,停止加热