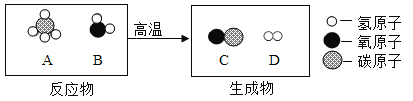
题目内容
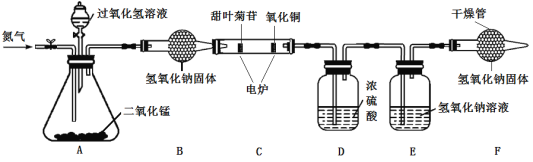
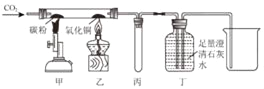
【题目】为了测定某氧化铁样品中氧化铁的质量分数,某化学小组设计了如图所示装置进行实验。

已知:样品中的杂质不含铁元素,且不溶于水和酸;草酸在浓硫酸作用下受热分解生成CO2、CO和H2O;碱石灰主要成分为生石灰与氢氧化钠固体。请回答:
(问题讨论)
(1)进入E中的气体是纯净、干燥的CO,则B、C、D中依次是________(填序号)。
①浓硫酸 ②氢氧化钠溶液 ③澄清石灰水
(2)B中发生反应的化学方程式为___________。
(3)C装置的作用是_________。
(数据处理)
(4)称取样品5.0 g,用上述装置进行实验,充分反应后称量F装置,发现比反应前增重3.3 g。则样品中氧化铁的质量分数为_______。
(实验反思)
(5)该实验装置有一明显缺陷是_______。
(6)如果没有G装置,则测得的样品中氧化铁的质量分数_______(填“偏大”、“偏小”或“无影响”)。
【答案】②③① 2NaOH+CO2═Na2CO3+H2O 检验二氧化碳是否被氢氧化钠溶液完全吸收 80% 没有处理尾气装置 偏大
【解析】
[问题讨论]
(1)由于进入E中的气体是纯净、干燥的CO,就要除去混合气体中的二氧化碳和水分;先用装置中氢氧化钠溶液除去混合气体中的二氧化碳,再用石灰水检验混合气体中的二氧化碳是否除净,最后用浓硫酸除去水分,故填②③①;
(2)B装置利用氢氧化钠吸收生成的二氧化碳,生成碳酸钠和水,故填2NaOH+CO2═Na2CO3+H2O;
(3)装置C盛放氢氧化钙溶液,检验二氧化碳是否被B装置完全吸收,故填检验二氧化碳是否被氢氧化钠溶液完全吸收;
[数据处理]
一氧化碳还原氧化铁生成铁和二氧化碳,所以F装置增加的重量就是反应生成的二氧化碳质量,即5.0g样品氧化铁被一氧化碳还原生成二氧化碳的质量是3.3g,设样品中氧化铁质量为X,
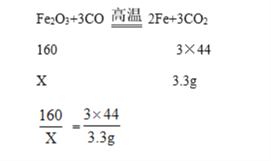
解得X=4.0g,样品中氧化铁质量分数=![]() ×100%=80%,故填80%;
×100%=80%,故填80%;
[实验反思]
(1)一氧化碳有毒,应该有尾气处理装置,故填没有尾气处理装置;
(2)如果没有G装置,F装置会吸收空气中的二氧化碳使测得的结果偏大,故填偏大。

 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案【题目】实验室常用的气体发生装置如图一所示。
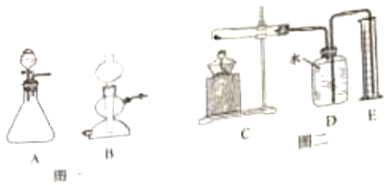
①实验室常用溶质质量分数为5%的过氧化氢溶液制取氧气,“5%”的含义是__。
②含溶质0.2mol的过氧化氢溶液完全分解,可以生成多少克氧气?___根据化学方程式列式计算),用5%的过氧化氢溶液和二氧化锰为原料制取氧气,较合理的发生装置是__(选填装置编号);
③探究溶质质量分数、催化剂质量、温度等因素对过氧化氢分解速率的影响,设计以下实验方案,其中实验甲、乙、丙的目的是__;实验戊中,w=__,t=__。
实验序号 | 过氧化氢溶液溶质质量分数 | 二氧化锰质量(g) | 温度(℃) |
甲 | 10% | 0.5 | 20 |
乙 | 10% | 1 | 20 |
丙 | 10% | 1.5 | 20 |
丁 | 5% | 1.5 | 30 |
戊 | w | 1.5 | t |
④加热氯酸钾和二氧化锰的混合物一段时间,测定生成氧气的体积,用图二所示装置进行实验(装置气密性良好)。试管中发生反应的化学方程式是__;有关该实验的说法合理的是__(选填编号)。
a.实验开始前装置D中必须装满水
b.连接C、D、E装置后点燃酒精灯
c.停止加热后,量筒内液面会下降
d.停止加热前应断开C、D装置,防止液体倒流