题目内容
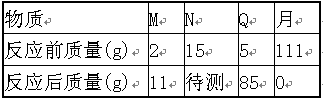
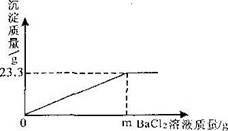
(6分)实验室中有一瓶存放时间过长的NaOH药品,其中一部分已转化为Na2C03。取lOg该药品放入烧杯中,加154g水配成溶液,将400g一定溶质质量分数的Ca(0H)2溶液分四次加人该烧杯中,充分反应后,测得生成沉淀质量的数据记录如下表:

(1)m=____g,
(2)求10g该药品中Na2C03的质量,
(3)第三次加入Ca(OH)2溶液充分反应后,所得溶液中溶质质量分数是多少?

(1)m=____g,
(2)求10g该药品中Na2C03的质量,
(3)第三次加入Ca(OH)2溶液充分反应后,所得溶液中溶质质量分数是多少?
(1)2
(2)解:根据题意知共生成CaCO3的质量为3g
设10g药品中含Na2CO3的质量为 X,同时生成 NaOH的质量为Y
Na2CO3 + Ca(OH)2 ="=" CaCO3↓+ 2NaOH
106 100 80
X 3 y
106/X=100/3=80/Y
X=3.18g Y=2.4g
(3)第三次反应后溶质NaOH 的质量=10-3.18+2.4=9.22g
第三次反应后溶液质量=154+10+300-3=461g
NaOH的质量分数为9.22/461ⅹ100%=2%
答:10g药品中含Na2CO3的质量为3.18g, 第三次反应后溶液中溶质质量分数2%。
(2)解:根据题意知共生成CaCO3的质量为3g
设10g药品中含Na2CO3的质量为 X,同时生成 NaOH的质量为Y
Na2CO3 + Ca(OH)2 ="=" CaCO3↓+ 2NaOH
106 100 80
X 3 y
106/X=100/3=80/Y
X=3.18g Y=2.4g
(3)第三次反应后溶质NaOH 的质量=10-3.18+2.4=9.22g
第三次反应后溶液质量=154+10+300-3=461g
NaOH的质量分数为9.22/461ⅹ100%=2%
答:10g药品中含Na2CO3的质量为3.18g, 第三次反应后溶液中溶质质量分数2%。
分析:分析表格可以发现,当生成3克沉淀时,碳酸钠全部参加反应,来求出碳酸钠的质量;
第三次加入氢氧化钙充分反应后,由于氢氧化钙和碳酸钠完全反应,所得溶液为氢氧化钠溶液;根据反应的化学方程式计算出反应生成氢氧化钠的质量,所得质量与溶液的质量比即得溶液的质量分数,反应后所得溶液的质量由质量守恒定律进行求得.
解答:解:(1)从第一次可以看出,加入100克氢氧化钙生成1克沉淀,因此当加入200克氢氧化钠,生成2克沉淀;
(2)有表格可知,第三次加入氢氧化钙时氢氧化钙和碳酸钠恰好完全反应,生成碳酸钙3g
设生成3g碳酸钙需用碳酸钠的质量为x,生成氢氧化钠质量为y
Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
106 100 80
x 3g y
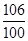 =
=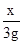 ,x=3.18g
,x=3.18g
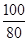 =
=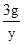 ,y=2.4g
,y=2.4g
10g该药品中碳酸钠的质量=3.18g.
(3)第三次加入氢氧化钙时,氢氧化钙和碳酸钠恰好完全反应,溶质为氢氧化钠,
氢氧化钠质量=10g-3.18g+2.4g=9.22g,溶液质量=154g+10g+300g-3g=461g,
溶液的质量分数=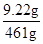 ×100%=2%.
×100%=2%.
答:(1)2;
(2)10g该药品中Na2CO3的质量为3.18g;
(3)第三次加入氢氧化钙溶液充分反应,所得溶液质量分数为2%.
点评:根据质量守恒定律,第三次加入氢氧化钙溶液充分反应后所得溶液的质量=参加反应溶液质量+三次所加氢氧化钙溶液的质量-反应生成的碳酸钙的质量;利用根据守恒定律化复杂的溶液计算为简便明了.
第三次加入氢氧化钙充分反应后,由于氢氧化钙和碳酸钠完全反应,所得溶液为氢氧化钠溶液;根据反应的化学方程式计算出反应生成氢氧化钠的质量,所得质量与溶液的质量比即得溶液的质量分数,反应后所得溶液的质量由质量守恒定律进行求得.
解答:解:(1)从第一次可以看出,加入100克氢氧化钙生成1克沉淀,因此当加入200克氢氧化钠,生成2克沉淀;
(2)有表格可知,第三次加入氢氧化钙时氢氧化钙和碳酸钠恰好完全反应,生成碳酸钙3g
设生成3g碳酸钙需用碳酸钠的质量为x,生成氢氧化钠质量为y
Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
106 100 80
x 3g y
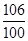 =
=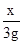 ,x=3.18g
,x=3.18g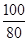 =
=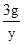 ,y=2.4g
,y=2.4g10g该药品中碳酸钠的质量=3.18g.
(3)第三次加入氢氧化钙时,氢氧化钙和碳酸钠恰好完全反应,溶质为氢氧化钠,
氢氧化钠质量=10g-3.18g+2.4g=9.22g,溶液质量=154g+10g+300g-3g=461g,
溶液的质量分数=
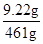 ×100%=2%.
×100%=2%.答:(1)2;
(2)10g该药品中Na2CO3的质量为3.18g;
(3)第三次加入氢氧化钙溶液充分反应,所得溶液质量分数为2%.
点评:根据质量守恒定律,第三次加入氢氧化钙溶液充分反应后所得溶液的质量=参加反应溶液质量+三次所加氢氧化钙溶液的质量-反应生成的碳酸钙的质量;利用根据守恒定律化复杂的溶液计算为简便明了.

练习册系列答案
相关题目