��Ŀ����
��3�֣�Ϊ�ⶨij̼������Ʒ���������ʲ�����ˮ�����ȣ�����������ʵ�飺ȡ48 g��Ʒ����ˮʹ̼������ȫ�ܽ���ȥ���ʣ����õ���Һ��ƽ����Ϊ�ķݣ�ÿ���зֱ����һ���������Ȼ�����Һ����Ӧ�Ļ�ѧ����ʽΪCaCl2 + Na2CO3 =" CaCO3��+" 2NaCl��ʵ�����ݼ��±���
����㣺
��ÿ��Һ����ȫ��Ӧʱ�����ɳ���������Ϊ �� g��
����Ʒ��̼���ƵĴ��ȡ�
| | ��һ�� | �ڶ��� | ������ | ���ķ� |
| ����CaCl2��Һ������/g | 10 | 20 | 30 | 40 |
| ���ɳ���������/g | 4 | 8 | 10 | 10 |
��ÿ��Һ����ȫ��Ӧʱ�����ɳ���������Ϊ �� g��
����Ʒ��̼���ƵĴ��ȡ�
��1��10
��2��88.3%
��: ��10 ����������������������������������������������1�֣�
������Ʒ��̼���Ƶ�����Ϊx��
CaCl2 + Na2CO3 =" CaCO3��+" 2NaCl ��
106 100
x 10 g��4

x��42.4 g ��������������������������1�֣�
��Ʒ��Na2CO3�Ĵ���= ������......��1�֣�
������......��1�֣�
����
������Ʒ��̼���Ƶ�����Ϊx��
CaCl2 + Na2CO3 =" CaCO3��+" 2NaCl ��
106 100
x 10 g��4

x��42.4 g ��������������������������1�֣�
��Ʒ��Na2CO3�Ĵ���=
 ������......��1�֣�
������......��1�֣�����

��ϰ��ϵ�д�
�����Ŀ
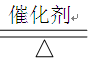 CH4 + 2H2O��������66 g������̼����ת�����õ�����������Ƕ��١�
CH4 + 2H2O��������66 g������̼����ת�����õ�����������Ƕ��١�