题目内容
 某实验小组的同学取大理石和稀盐酸反应后的废液50g,逐滴加入质量分数为26.5%的碳酸钠溶液.他们根据实验测得的数据绘出右图,其中纵坐标m是实验得到的沉淀或气体的质量,横坐标表示的是碳酸钠溶液质量.下列说法正确的是( )
某实验小组的同学取大理石和稀盐酸反应后的废液50g,逐滴加入质量分数为26.5%的碳酸钠溶液.他们根据实验测得的数据绘出右图,其中纵坐标m是实验得到的沉淀或气体的质量,横坐标表示的是碳酸钠溶液质量.下列说法正确的是( )A.图中oa段表示生成的沉淀量
B.c点表示碳酸钠合好完全反应
C.与50g废液恰好完全反应时消耗碳酸钠溶液的质量为30g
D.最终产生气体的质量为5g
【答案】分析:根据右图可知碳酸钙与盐酸反应后盐酸过量,所以一开始没有产生沉淀原因是加入的碳酸钠先与盐酸反应,把盐酸消耗完了,才开始与氯化钙反应,开始生成沉淀,最后到达最高点说明已经反应完了.
解答:解:A、图中oa段表示生成的气体质量,故A错;
B、b点表示碳酸钠恰好完全反应,故B错;
C、根据题意可知碳酸钠先与盐酸反应,再与氯化钙反应,由图示可知10g碳酸钠与盐酸反应,20g碳酸钠与氯化钙反应,所以共消耗碳酸钠溶液30g,故C正确;
D、最终产生气体质量为2.2g,故D错.
故选C.
点评:解答本题关键要知道只有把盐酸反应完了,才能与氯化钙反应产生沉淀,因为如果碳酸钠与氯化钙先反应生成了碳酸钙沉淀,也会被剩余的盐酸溶解掉,将不会看到沉淀.
解答:解:A、图中oa段表示生成的气体质量,故A错;
B、b点表示碳酸钠恰好完全反应,故B错;
C、根据题意可知碳酸钠先与盐酸反应,再与氯化钙反应,由图示可知10g碳酸钠与盐酸反应,20g碳酸钠与氯化钙反应,所以共消耗碳酸钠溶液30g,故C正确;
D、最终产生气体质量为2.2g,故D错.
故选C.
点评:解答本题关键要知道只有把盐酸反应完了,才能与氯化钙反应产生沉淀,因为如果碳酸钠与氯化钙先反应生成了碳酸钙沉淀,也会被剩余的盐酸溶解掉,将不会看到沉淀.

练习册系列答案
相关题目
 同学们在探究碱溶液与酚酞溶液作用的实验时,发现了一个意外现象:向氢氧化钠溶液中滴入酚酞溶液(如图),溶液变成了红色,但是一会儿红色就消失了.为此某化学小组的同学进行了如下探究.
同学们在探究碱溶液与酚酞溶液作用的实验时,发现了一个意外现象:向氢氧化钠溶液中滴入酚酞溶液(如图),溶液变成了红色,但是一会儿红色就消失了.为此某化学小组的同学进行了如下探究.【提出猜想】甲:可能是酚酞溶液变质的缘故
乙:可能是氢氧化钠溶液与空气中二氧化碳反应的缘故
丙:可能是氢氧化钠与酚酞混合后与空气中氧气反应,使红色消失的缘故
丁:可能与氢氧化钠溶液的质量分数有关
【查阅资料】酚酞是一种常用酸碱指示剂,遇碱性溶液变红.
【讨论分析】(1)甲同学提出猜想后,很快被小组同学否定了,其理由是
(2)经过思考,大家认为乙同学的猜想也不正确,其理由是
(3)为验证丙同学的猜想是否正确,小组同学做了如下实验,请完成表中内容.
| 实验步骤 | 实验目的 | 现象结论 |
| ①用煮沸过的蒸馏水配制某氢氧化钠溶液. | 溶液先变成红色,一会儿红色又消失. 丙同学的猜想不正确. | |
| ②取少量上述氢氧化钠溶液,滴入酚酞,然后在上方滴一些植物油. |
| 实验方法 | 观察到的现象和结论 |
| 方案一:分别配制不同质量分数的氢氧化钠溶液,然后各取少量并滴加2滴酚酞溶液. | 质量分数小的溶液中红色不消失,质量分数大的溶液中红色会消失,则证明 |
| 方案二: |
出现红色且不褪去,结论同上. |
A.10% B.15% C.20% D.30%
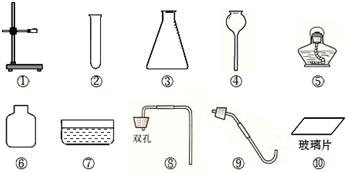 26、实验室提供了以下仪器,请你随某兴趣小组的同学一起来参加实验探究活动:
26、实验室提供了以下仪器,请你随某兴趣小组的同学一起来参加实验探究活动: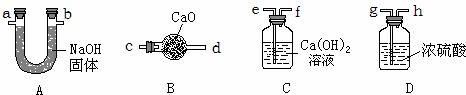
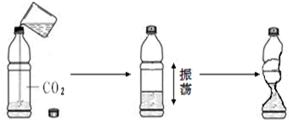


 (2012?南通)维生素C是一种人体必需的维生素.查阅资料可知下列信息:
(2012?南通)维生素C是一种人体必需的维生素.查阅资料可知下列信息: