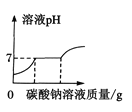
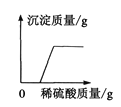
��Ŀ����
����Ŀ��SO2��CO2�Ĵ����ŷŷֱ���������������ЧӦ��ֱ��ԭ��SO2��CO2�Ƚϣ�����������һЩ��ͬ�㣬�磺�ܶȶ��ȿ�������ʹ����ʯ��ˮ����ǵȣ�Ҳ�в�ͬ�㣬�磺SO2��ǿ�ҵĴ̼�����ζ�����ж���SO2��ʹƷ����Һ��ɫ�������й�˵������ȷ���ǣ�������
A.����Ʒ����Һ����SO2��CO2
B.SO2��CO2��������Ԫ�ص�������������ͬ
C.ij��ɫ����ͨ�����ʯ��ˮ�У�ʯ��ˮ����ǣ�������һ����CO2
D.ij��ɫ����ͨ�����ʯ��ˮ�У�ʯ��ˮ����ǣ������岻һ����CO2
���𰸡�C
��������
������֪��SO2��CO2�Ƚϣ�����������һЩ��ͬ�㣬�磺�ܶȶ��ȿ�������ʹ����ʯ��ˮ����ǵȣ�Ҳ�в�ͬ�㣬�磺SO2��ǿ�ҵĴ̼�����ζ�����ж���SO2��ʹƷ����Һ��ɫ�������ѡ����Ǹ�����Щ�������жϡ�
A������SO2��CO2���������ʾ����ģ�����Ʒ����Һ����SO2��CO2����A��ȷ��
B��SO2��������Ԫ�ص�����������![]() ��CO2��������Ԫ�ص���������
��CO2��������Ԫ�ص���������![]() ���ɼ�SO2��CO2��������Ԫ�ص�������������ͬ����B��ȷ��
���ɼ�SO2��CO2��������Ԫ�ص�������������ͬ����B��ȷ��
C��SO2ͨ������ʯ��ˮ����������Ƴ��������Ի�ʹ�����ʯ��ˮ����ǣ�CO2ͨ������ʯ��ˮ����̼��Ƴ��������Ի�ʹ�����ʯ��ˮ����ǣ���C����
D����C�Ľ�����֪��D��˵����ȷ��
��ѡC��

����Ŀ��̽��þ��п������ͭ���ֽ����ܷ����ᷴӦ
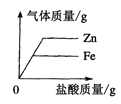
(1)��������ͼ��ʾ��ʵ��,��ش����⣺
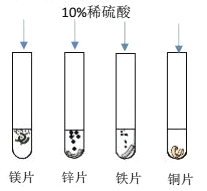
������֧�Թ��в�����ʵ������IJ�ͬ�ɻ�֪���ֽ����Ļ����ǿ������˳����______����ϡ�������ʱ,װ����Ƭ���Թ��з�Ӧ�����Һ���е�������_______(�����ӷ��ű�ʾ)��
(2)�������������ᷴӦ���ڸ��ֹ���,��������±��е�����,�ҵ���Ӧ��ϵ��
lg����������ϡ�ν�����������������+2�۽���������Һ�� | þ | п | �� |
���������ԭ������ | 24 | 65 | 56 |
����������������g�� | 2/24 | 2/65 | 2/56 |
�㷢�ֵĹ��� | _______ | ||
����չӦ�ã�
������������ƻƽ�Ģ�Cu-Zn�Ͻ�͢�Cu-Ag��Ʒ,��ʵ����ֻ�ṩһƿϡ����ͱ�Ҫ������
(3)����Ϊ�ܲ���Ͻ�________(�����)��ͭ������������
(4)ȡ����(3)����ѡ�Ͻ��ĩ20g�����ձ���,����50g��ϡ����,ǡ����ȫ��Ӧ,����ձ���ʣ�����ʵ�����Ϊ69.8g,��:
�ٲ���������������________��
�ڸúϽ���ͭ����������Ϊ_____________��