题目内容
【题目】下图中A、B、C、D为四种粒子的微粒结构示意图,E为钙元素在周期表中的信息。请按要求填空:
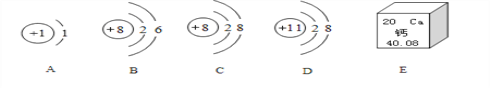
(1)在A、B、C、D中共表示____种元素的粒子;具有相对稳定结构的粒子是______;表示阳离子的是_________。
(2)A的单质在B的单质中燃烧的化学方程式是_________。
(3) E中钙原子的相对原子质量是____________。
【答案】 3或者三 CD D 2H2 + O2![]() 2H2O 40.08
2H2O 40.08
【解析】(1)A、B、C、D共表示三种元素的粒子;CD的离子最外层电子数相同,都具有稳定的结构;D的核内质子数>核外电子数,属于阳离子;(2) A的单质是氢气,B的单质是氧气,故A的单质在B的单质中燃烧的化学方程式是:2H2+O2 ![]() 2H2O;(3)从E图可以看出,钙原子的相对原子质量是40.08。
2H2O;(3)从E图可以看出,钙原子的相对原子质量是40.08。

 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案【题目】兴趣小组的同学对碳酸氢钠、碳酸钠、氢氧化钠的某些性质进行相关探究。
[提出问题] 它们溶液的酸碱性及与酸反应时溶液的pH如何变化?
[实验探究1] 向等体积、等浓度的碳酸氢钠、碳酸钠、氢氧化钠溶液中,分别加入几滴紫甘蓝汁液,同时用蒸馏水进行对比实验,观察并记录现象如下表:
液体名称 | 蒸馏水 | 碳酸氢钠溶液 | 碳酸钠 溶液 | 氢氧化钠溶液 |
紫甘蓝汁液显示的颜色 | 蓝紫色 | 蓝色 | 绿色 | 黄色 |
查阅资料:
pH | 7.5~9 | 10~11.9 | 12~14 |
紫甘蓝汁液 显示的颜色 | 蓝色 | 绿色 | 黄色 |
[得出结论1] 三种溶液的碱性由强到弱的顺序为______________________。
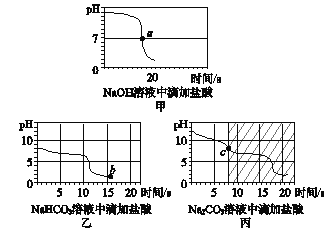
[实验探究2] 甲同学在烧杯中加入约5 mL稀氢氧化钠溶液,滴入几滴酚酞溶液,此时溶液由______色变为________色。向其中加入稀盐酸,该反应的化学方程式为___________。乙同学向一定体积、一定浓度的氢氧化钠溶液中,逐滴加入一定浓度的盐酸,得到pH变化与时间的关系如下图甲所示。a点表示的含义是________________。
[得出结论2] 从微观角度分析,该反应的实质是_____________________。
[实验探究3] 向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入一定浓度的盐酸,得到pH变化与时间的关系如图乙、图丙所示。
[交流与反思] b点的溶质为____________________。(填化学式),将图乙和图丙中的阴影部分进行叠加,发现两者基本重合,c点的溶质为____________(填化学式)。
[得出结论3] 通过上述分析,碳酸钠和盐酸反应过程,可以依次用以下两个化学方程式表示:______、______________。
[结论与反思] 探究溶液的酸碱性及反应pH的变化,可以认识反应的原理及进行的过程。