题目内容
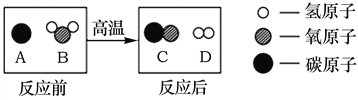
【题目】下列是初中化学中的一些常见实验,请回答相关问题。
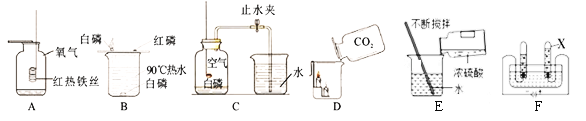
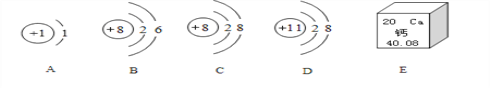
(1)A中的实验现象是_______________________;
(2)从B实验能得出燃烧条件之一是______________;
(3)C实验测定空气中氧气含量过程中,导致实验结果偏小的原因可能是_________(写一点)。
(4)通过D实验对CO2气体从物理性质和化学性质两个方面得到结论:物理性质___________(填一条即可),化学性质__________________(填一条即可)。
(5)E实验浓硫酸的稀释实验中,用玻璃棒搅拌的目的___________。
(6)F电解水实验中,在水中加入硫酸钠的作用是__________,X管中产生的气体是_______。
【答案】 剧烈燃烧、火星四射、生成黑色固体。同时放出大量的热 可燃物必须与氧气接触(或温度达到着火点) 红磷量不足(合理即可) 密度比空气大 不能燃烧(不能支持燃烧) 搅拌使热量散失 增强水的导电性 氧气
【解析】本题考查了燃烧的条件探究,空气组成的测定,氧气的化学性质;二氧化碳的性质,浓硫酸的稀释,水的电解实验等。
(1)铁丝在氧气中剧烈燃烧、火星四射、生成黑色固体。同时放出大量的热;
(2)B实验中铜片上的白磷燃烧,热水中的白磷没有燃烧,由此可知,可燃物燃烧的条件之一是与氧气接触;铜片上的白磷燃烧,红磷不燃烧,二者均与氧气接触,由此可知,可燃物燃烧的条件之一是温度达到可燃物的着火点;
(3)C实验测定空气中氧气含量过程中,导致实验结果偏小的原因可能是红磷量不足(合理即可);
(4)蜡烛能够熄灭说明了二氧化碳既不能燃烧也不支持燃烧,低处蜡烛先灭,高处蜡烛后熄灭,说明二氧化碳先聚集在低处,说明了二氧化碳的密度比空气的密度大;
(5)浓硫酸溶于水时放出大量热。E实验浓硫酸的稀释实验中,用玻璃棒搅拌的目的搅拌使热量散失;
(6)水的导电性较弱,硫酸钠在水中能离解出可自由移动的钠离子和硫酸根离子。F电解水实验中,在水中加入硫酸钠的作用是增强水的导电性,X管与电源的正极相连,产生的气体是氧气。

【题目】某种矿石由氧化镁、氧化铁、氧化铜和二氧化硅组成,用它制备氢氧化镁的流程示意图如图所示(已知:二氧化硅不溶于水也不与稀盐酸反应)。
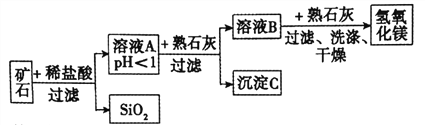
请回答下列问题。
(1)加稀盐酸之前要将矿石粉碎的目的是_____________。
(2)溶液A中除了Mg2+外,还含有的金属阳离子是______________;(写离子符号)
写出矿石中的任意一种金属氧化物与稀盐酸反应的化学方程式:______________(只写一个)。
(3)在溶液A中加入熟石灰调节溶液的pH,可以使溶液中的金属阳离子逐步转化为沉淀。该实验条件下,使金属阳离子沉淀的相关pH数据见下表。为保证产品纯度、减少产品损失,并便于操作,所得溶液B的pH的取值范围为______________。(用不等式表示)
氢氧化物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
开始沉淀的pH | 1.5 | 4.2 | 8.6 |
完全沉淀的pH | 3.2 | 6.7 | 11.1 |
(4)写出溶液B中加入熟石灰发生反应的化学方程式:___________________________。