题目内容
【题目】某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时 有较多的气泡放出,生成的是什么气体呢?同学们决定进行探究,探究前老师提示,该反应 生成的气体只有一种。
(提出猜想)放出的气体可能是 SO2、O2、H2,提出猜想的依据是__________________;
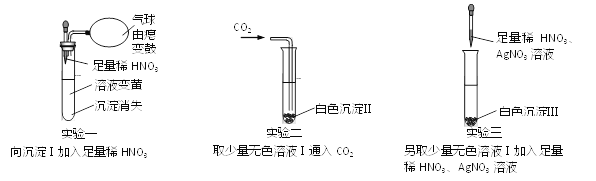
(查阅资料)SO2 易溶于水,化学性质与二氧化碳有相似之处,它能使澄清石灰水变浑浊, 生成 CaSO3。
(方案设计)根据上述猜想,实验小组同学分别设计了如下方案:
(1)甲同学认为是 O2,则检验方法是______________________;
(2)SO2 是一种空气污染物,容易形成酸雨,试写出酸雨的一种危害_____,乙 同学认为是 SO2,可用氢氧化钠溶液吸收,写出该反应的化学方程式________;
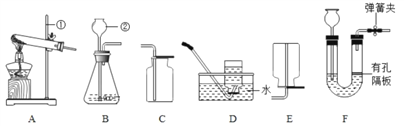
(3)实验小组同学合作了如下组合实验方案,排除和验证猜想的气体。
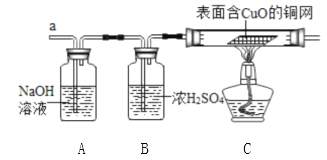
实验开始时,先将收集到的气体从 a 通入一段时间后,再点燃 B 处酒精灯,这样操作的目的是__ ,实验小组的同学在实验过程中发现 A 装置中溶液不变浑浊,B 装置中表面含 CuO 的铜网由黑色变为光亮的红色;根据现象,你 认为硫酸铜溶液中一定含有的离子是__________ 。
【答案】 质量守恒定律,根据反应前后元素种类不变判断 可用带火星的木条检验,若木条复燃为氧气 腐蚀建筑物和工业设备(其他合理答案均可) SO2+2NaOH = Na2SO3+H2O 将装置内的空气排出,防止发生爆炸。 H+
【解析】本题考查了质量守恒定律,氧气、氢气的检验,碱的性质等。首先分析题中考查的问题,然后结合所给的知识和学过的知识进行分析解答。
提出猜想:铁粉投入硫酸铜溶液中,反应前含有S、O、H、Cu元素,依据质量守恒定律,根据反应前后元素种类不变判断可以得出猜想;
方案设计:(1)氧气具有助燃性,可以通过检验气体的助燃效果进行判断。检验方法是用带火星的木条检验,若木条复燃为氧气;
(2)SO2 是一种空气污染物,容易形成酸雨,酸雨的一种危害腐蚀建筑物和工业设备等;二氧化硫和氢氧化钠反应会生成亚硫酸钠和水,该反应的化学方程式是SO2+2NaOH = Na2SO3+H2O;
(3)实验探究:可燃性的气体和空气混合加热时可能会发生爆炸,因此先将收集到的气体从a通入一段时间后,再点燃C处酒精灯的目的是排出装置内的空气,以防加热时爆炸;A处的氢氧化钠将产生的SO2吸收,B中浓硫酸将水蒸气吸收。H2可以使CuO还原成红色的Cu,所以产生的气体为氢气,硫酸铜溶液中一定含有的离子是H+。

【题目】图表法是一种常用的数据处理方法,根据所给图表(氢氧化钠、碳酸钠分别在水、酒精中的溶解度如表所示),下列说法正确的是( )
氢氧化钠 | 碳酸钠 | |||
20℃ | 40℃ | 20℃ | 40℃ | |
水 | 109g | 129g | 21.8g | 49g |
酒精 | 17.3g | 40g | 不溶 | 不溶 |

A. 上述图象表示碳酸钠的溶解度曲线
B. 20℃时,氢氧化钠的溶解度大于碳酸钠
C. 40℃时,若将 50g NaOH 分别投入到 100g 水和 100g 酒精中,都能形成饱和溶液
D. 40℃时,将适量 CO2 通入饱和的 NaOH 酒精溶液中,观察不到明显的现象
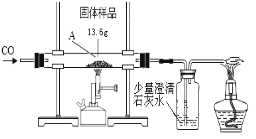
【题目】某化学兴趣小组的同学对一份固体样品进行了探究。通过实验已确定该样品由氧化铁和铁粉混合而成。他们称取了13.6g固体样品,用下图所示的装置继续实验,完全反应后,测定的有关数据如下表所示。
A中固体 的质量 | 澄清石灰水 的质量 | |
反应前 | 13.6g | 102.5g |
反应后 | 11.2g | 108.0g |
请计算:
⑴实验中先通CO的目的是____________________________________。
⑵从上表中选择合适的数据,计算固体样品中氧化铁的质量是_____________克。
⑶在上述反应后的固体中加入100g稀盐酸,恰好完全反应,求反应后所得溶液中溶质的质量分数___。(请写出完整计算过程,结果精确到0.1%)