题目内容
【题目】某化学兴趣小组的同学对一份固体样品进行了探究。通过实验已确定该样品由氧化铁和铁粉混合而成。他们称取了13.6g固体样品,用下图所示的装置继续实验,完全反应后,测定的有关数据如下表所示。
A中固体 的质量 | 澄清石灰水 的质量 | |
反应前 | 13.6g | 102.5g |
反应后 | 11.2g | 108.0g |
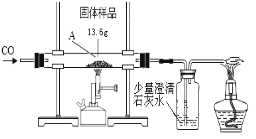
请计算:
⑴实验中先通CO的目的是____________________________________。
⑵从上表中选择合适的数据,计算固体样品中氧化铁的质量是_____________克。
⑶在上述反应后的固体中加入100g稀盐酸,恰好完全反应,求反应后所得溶液中溶质的质量分数___。(请写出完整计算过程,结果精确到0.1%)
【答案】 除去装置内的空气,防止加热时引起爆炸 8 22.9%
【解析】(1)由于一氧化碳具有可燃性,不纯点燃可能引起爆炸,所以实验中先通CO,除去装置内的空气;
(2)因为少量澄清石灰水不能将生成的二氧化碳完全吸收,所以应该选择A中固体的质量变化进行计算,固体减少的质量为13.6g-11.2g=2.4g,即为氧化铁中氧元素的质量,
设氧化铁的质量为x,
Fe2O3+3CO ![]() 2Fe+3CO2 固体减重
2Fe+3CO2 固体减重
160 112 160-112=48
y (13.6g-11.2 g)=2.4g
![]()
解得x=8g
⑶设生成的FeCl2和H2质量分别为y、z,
Fe + 2HCl =FeCl2 + H2↑
56 127 2
11.2g y z
![]()
解得y=25.4g ,z=0.4g
则反应后的溶液中溶质的质量分数为![]() ×100%≈22.9%。
×100%≈22.9%。
答:反应后的溶液中溶质的质量分数为22.9%。

练习册系列答案
相关题目