题目内容
【题目】根据如图回答问题:
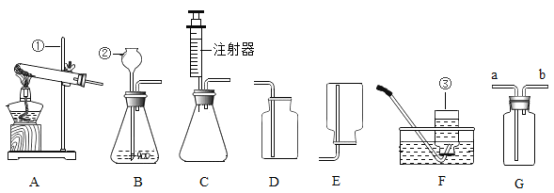
(1)装置的仪器名称是①_____,②_____。
(2)实验室用高锰酸钾制氧气时,应选用的发生装置____(填字母代号),需要对装置进行改进是____,若用装置G收集氧气,验满的方法是____。
(3)实验室制取二氧化碳的化学方程式为____。
(4)实验室通常不用碳酸钠与稀盐酸反应来制取二氧化碳,因为反应速率太快,不利于气体收集,但若用装置C则可以,与装置B比较,C装置的优点是_____。为检验是否有二氧化碳生成,某同学将制得的气体通入到紫色石蕊溶液中,你认为该操作____(填“可行”或“不可行”)。
(5)氨气(NH3)是一种密度比空气小,极易溶于水的气体,实验室常用固体NH4Cl和固体Ca(OH)2加热制得NH3。同时得到氯化钙和水,实验室制取和收集NH3应该选用上述仪器中的____(填序号)。
【答案】铁架台 长颈漏斗 A 试管口塞一团棉花 带火星的木条放在b管口,木条复燃,说明已收集满 CaCO3+2HCl=CaCl2+CO2↑+H2O 可以控制反应物的用量、控制反应的速率 不可行 AE
【解析】
高锰酸钾加热生成锰酸钾、二氧化锰和氧气,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,实验室常用固体NH4Cl和固体Ca(OH)2加热制得NH3。同时得到氯化钙和水。
(1)装置的仪器名称是①是铁架台,②是长颈漏斗。
(2)高锰酸钾加热生成锰酸钾、二氧化锰和氧气,实验室用高锰酸钾制氧气时,应选用的发生装置A,高锰酸钾是粉末状的,为防止高锰酸钾粉末进入导管,需要对装置进行改进是试管口塞一团棉花,若用装置G收集氧气,氧气具有助燃性,故验满的方法是带火星的木条放在b管口,木条复燃,说明已收集满。
(3)碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,故实验室制取二氧化碳的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O。
(4) 装置C含有针筒,可以控制反应物的用量,控制反应的速率,若用装置C则可以,与装置B比较,C装置的优点是可以控制反应物的用量、控制反应的速率。二氧化碳气体中可能带有挥发出的氯化氢气体,氯化氢溶于水形成盐酸,能使紫色石蕊溶液变红,故该操作不可行。
(5) 实验室常用固体NH4Cl和固体Ca(OH)2加热制得NH3。同时得到氯化钙和水,反应需要加热,则发生装置选用A,氨气(NH3)是一种密度比空气小,极易溶于水的气体,用向下排空气法收集,收集装置选用E,故实验室制取和收集NH3应该选用上述仪器中的AE。

 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案【题目】常温下,H2O2分解生成O2的速率较为缓慢。研究性学习小组选择“H2O2分解生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
(提出假设)催化剂的种类会影响H2O2分解生成O2的快慢。
(供选择的试剂)5%H2O2溶液、15%H2O2溶液、30%H2O2溶液、二氧化锰粉末、二氧化锰颗粒、氧化铜粉末
(设计方案)常温下,取两份5%H2O2溶液各100mL,分别加入_________,测量各生成一瓶相同O2所需的时间。
(实验探究)如图是他们进行实验的装置图,此实验中A处宜采用的气体收集方法是______。检查装置气密性良好,将分液漏斗中的液体加入锥形瓶中,立即收集一瓶气体。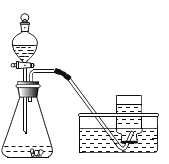
(实验记录)
实验编号 | ① | ② |
反应物 | 5%H2O2溶液100mL | 5%H2O2溶液100mL |
加入固体 | CuO | MnO2 |
收集一瓶气体所需时间 | 165s | 46s |
(实验分析)(1)若要证明二氧化锰、氧化铜是该反应的催化剂,还需要验证它们在化学反应前后的___和___没有改变。
(2)要定量地比较化学反应速度的快慢,除了上述方法外,还可以_________。
(得出结论)该探究过程得出的结论是____________,故实验室用H2O2溶液制取氧气的化学方程式为________。
(反思)还有哪些因素可能影响该反应的速率呢?
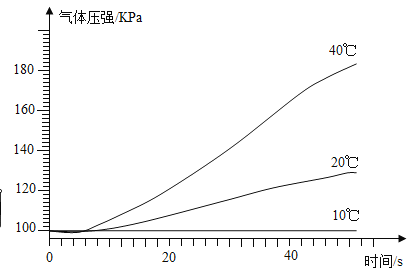
(1)在老师的帮助下,小组同学们使用压强传感器气体压强等设备,探究在其他条件相同时,不同温度下过氧化氢溶液分解时密闭容器内压强的变化。经过实验数据处理等,获得如图所示的压强-时间的曲线变化图。由此得出的结论是___________。
(2)你还有其他的猜想吗?
猜想:_____________。
请选择题目中提供的试剂,设计实验证明你的猜想(包括实验方案和结论)_____________。
【题目】化学兴趣小组为了测定一批石灰石样品中碳酸钙的质量分数,取用2g石灰石样品,把20g稀盐酸(氯化氢的水溶液)分4次加入样品中(样品中除碳酸钙外,其余成分既不与盐酸反应,也不溶解于水),充分反应后经过滤、千燥等操作,最后称量,得实验数据如下:
稀盐酸的用量 | 剩余固体的质量 |
第一次加入5.0g | 1.4g |
第二次加入5.0g | 0.8g |
第三次加入5.0g | 0.2g |
第四次加入5.0g | 0.2g |
(1)从以上数据可知,这四次实验中,第________________次石灰石样品中碳酸钙已完全反应,判断的依据是__________________。
(2)求该石灰石样品与稀盐酸反应产生的二氧化碳质量。______