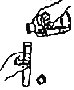题目内容
【题目】丙烷(C3H8)是液化石油气的主要成分之一,燃烧产物与甲烷相同。
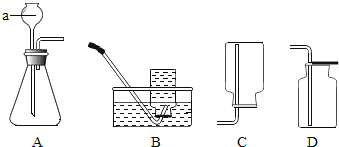
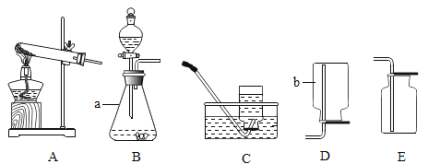
(1)图中仪器a的名称是_____。
(2)请写出丙烷在空气中完全燃烧的化学方程式:_____。
(3)纯净的丙烷无色无味,为防泄漏,需在家中安装报警器。你所选择的安装位置是_____(填地面或者天花板)。
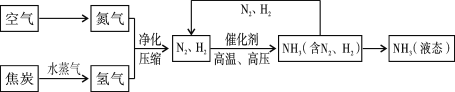
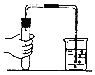
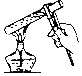
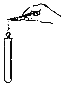
(4)相比于液化石油气,氢气是种更为理想的能源。实验室制取并收集氢气,可选择_____(填字母代号)装置。
【答案】长颈漏斗 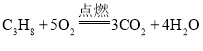 地面 AB或AC
地面 AB或AC
【解析】
(1)图中仪器a的名称是长颈漏斗;
(2)丙烷燃烧生成二氧化碳和水,其化学方程式为: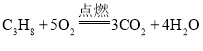 ;
;
(3)丙烷相对分子质量为(12×3)+(1×8)=44,密度比空气大,泄漏后会沉往地面,报警器应该安装在地面;
(4)实验室用锌和稀硫酸制取氢气,该反应不需加热,属于固液混合常温型,故应选择的发生装置是 A;由于氢气的密度比空气小,用向下排空气法收集,难溶于水可以用排水法收集,收集装置可选B或C,故可选择AB或AC装置。

【题目】某实验小组将少量氢化钙(CaH2)溶于水,形成了无色透明的溶液,再向其中加入碳酸钠溶液,有沉淀产生,经过滤后得到滤渣和滤液。然后进行了滤渣验证和滤液溶质成分的探究。
(1)(查阅资料)氢化钙在常温下能与水反应生成氢氧化钙和氢气,写出该反应的化学方程式______________。
(2)(交流验证)滤渣只能是碳酸钙,用盐酸验证此滤渣的化学方程式为______________。
(3)(提出问题)滤液中溶质的成分是什么?
(4)(猜想假设)猜想一:NaOH
猜想二:NaOH和Na2CO3
猜想三:NaOH和________。
猜想四:NaOH、Na2CO3和Ca(OH)2
(5)(讨论分析)经过讨论认为最不合理的是猜想____,原因是______________。
(6)(实验与结论)
实验步骤 | 现象 | 结论 |
步骤I:取少量滤液,向其中加入足量盐酸溶液 | ________ | 猜想二不成立 |
步骤Ⅱ:另取少量滤液,向其中滴入适量Na2CO3溶液 | 产生白色沉淀 | 猜想____成立 |
(7)(拓展延伸)在分析反应后所得物质的成分时,除考虑生成物外,还需考虑___________。