题目内容
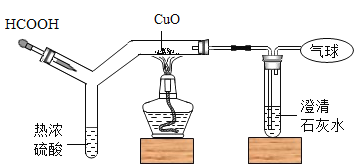
【题目】合成氨是人类科学技术上得一项重大突破,对社会发展与进步做出了巨大贡献。合成氨的工艺流程图如下:
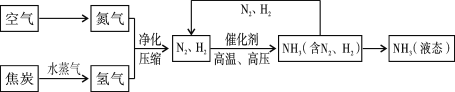
(1)合成氨需要的氮气来自空气,空气中氮气的体积分数约为_______,工业上采用分离液态空气的方法制取氧气,该方法属于_________(填“物理”或“化学”)变化。
(2)制取氢气的反应过程为: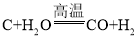 ;
;![]() ;上述两个化学方程式中表现氧化性的物质是_____________(填化学式)。
;上述两个化学方程式中表现氧化性的物质是_____________(填化学式)。
(3)原料中N2、H2中常含有CO2和水蒸气,反应前要净化。净化过程中所用两种试剂的先后顺序为_____。
(4)写出N2、H2反应生成NH3的化学方程式_________。
(5)该流程中产生可循环使用的物质是___________________。
【答案】78% 物理 H2O 先把原料气通过NaOH溶液,再通过浓硫酸  N2 H2
N2 H2
【解析】
(1)合成氨需要的氮气来自空气,空气中氮气的体积分数约为78%,工业上采用分离液态空气的方法制取氧气,该方法中没有新物质生成,属于物理变化。
(2)水在上述两个化学方程式中,提供氧元素,表现为氧化性,水的化学式为H2O。
(3)在除杂和干燥时,应除杂后干燥,所以先把原料气通过碱石灰除掉二氧化碳,再通过浓硫酸除掉水分,净化过程中所用两种试剂的先后顺序为:先把原料气通过NaOH溶液,再通过浓硫酸;
(4)氮气和氢气在有催化剂和高温高压的条件下生成氨气,反应的化学方程式为 ;
;
(5)由图可知:上述流程中可循环利用的物质是N2 H2。

【题目】金属防腐是科学研究中的重大课题。某校学习小组以铁的腐蚀为项目进行如下研究。
(认识铁的腐蚀)
(1)下列环境中的铁制品最容易生锈的是_______(填字母序号)。
A 未擦干的铁锅 B 除油漆的栏杆 C 盛水的不锈钢水杯
(2)铁锈的主要成分是Fe2O3·xH2O,其中铁元素的化合价是____。
(探究铁的腐蚀)
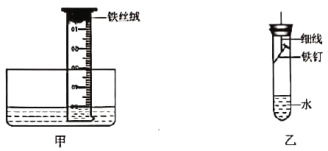
(3)该小组用下图甲装置进行实验,起始时量筒内水面处于50 mL刻度处,之后水面缓慢上升。几天后水面最终处于约____(填“40”或“10”)mL刻度处,原因是____。
(拓展探究)
(4)小强同学进行如下实验:取铁钉用砂纸打磨,称其质量,按上图乙安装装置,放置3天,再取出铁钉称量。在不同温度下重复上述实验,得到铁钉质量增加情况如下表。
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
铁钉质量增加/g | 0.02 | 0.04 | 0.08 | 0.16 | 0.18 | 0.18 | 0.18 |
小强同学的实验是探究____因素对铁钉腐蚀快慢的影响,结论是____。
(5)有同学认为小强的实验未能真实反映50℃以后铁钉腐蚀的快慢,理由是50℃以后铁钉质量没有变化。请分析铁钉质量没有变化的原因:____;改进实验方案证明你的____。
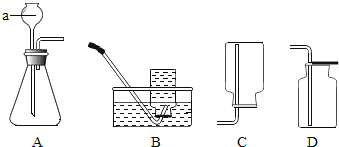
【题目】为测定锌铜合金中锌的含量,取该合金放入如图 14 盛有稀硫酸的锥形瓶中,发生反应: Zn+H2SO4=ZnSO4+H2↑ 。多次实验后,取平均值所得数据如下表:

反应前 | 充分反应后装置及反应剩余物质质量 | |
装置和足量的稀硫酸质量 | 锌铜合金质量 | |
342.10g | 16.00g | 357.70g |
若不考虑干燥剂吸收空气中的水蒸气,计算:
(1)根据质量守恒定律求生成氢气的质量。
(2)该合金中锌的质量分数。