题目内容
【题目】利用高锰酸钾制取氧气并测定室温下氧气的密度,实验步骤如下:

①组装实验装置。
②_____。
③把适量的高锰酸钾粉末放入试管中,称量试管与高锰酸钾粉末的质量为 m g。
④加热,开始反应,直到产生一定量的气体。
⑤停止加热,冷却到室温。
⑥测量收集到的气体体积。
⑦称量试管和残留物的质量为 n g。
回答下列问题:
(1)图中的 a 仪器名称_____。
(2)实验步骤的第②步是_____。
(3)写出试管发生反应的化学方程式:_____。
(4)选用制取气体的发生装置需考虑反应物的状态和_____。
(5)该方法能测量收集到的氧气体积,是依据氧气_____的性质。如果实验中得到的氧气体积是 V L,水蒸气的影响忽略不计,则室温下氧气密度的计算式为_____。
(6)假定其他操作均正确,未恢复至室温就读数会导致实验结果_____(填“偏大”、“偏小”或“无影响”)。
【答案】铁架台 检查装置气密性 2KMnO4![]() K2MnO4+MnO2+O2↑ 反应条件 不易溶于水
K2MnO4+MnO2+O2↑ 反应条件 不易溶于水 ![]() 偏小
偏小
【解析】
解:实验步骤如下:①组装实验装置。②检查装置气密性。
(1)图中的 a 仪器名称是铁架台。
(2)实验步骤的第②步是检查装置气密性。
(3)试管中高锰酸钾分解生成锰酸钾、二氧化锰和氧气,发生反应的化学方程式:2KMnO4![]() K2MnO4+MnO2+O2↑。
K2MnO4+MnO2+O2↑。
(4)选用制取气体的发生装置需考虑反应物的状态和反应条件。
(5)该方法能测量收集到的氧气体积,是依据氧气不易溶于水的性质;
如果实验中得到的氧气体积是 V L,水蒸气的影响忽略不计,则室温下氧气密度的计算式为:![]() 。
。
(6)假定其他操作均正确,未恢复至室温就读数会导致氧气体积偏大,从而导致实验结果偏小。

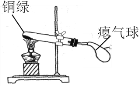
【题目】兴趣小组同学发现实验室一片久置的铜片表面附着有一层绿色固体,查阅资料得知绿色固体是铜绿 [化学式为Cu2(OH)2CO3],甲同学从铜片上刮下一些铜绿进行如下探究,请填写下表中空白:
实验步骤 | 实验现象 | 实验结论 |
| 试管内壁有水雾。 | 铜绿加热产生_________。 |
_________________。 | 铜绿加热后生成氧化铜。 | |
气球胀大。 |
乙同学对气球胀大产生兴趣,于是进行了如下的探究。
(发现问题) 气球为什么会胀大?
(提出猜想) 猜想Ⅰ:试管内的空气受热膨胀使气球胀大;
猜想Ⅱ:铜绿加热产生二氧化碳使气球胀大;
猜想Ⅲ:铜绿加热产生一氧化碳使气球胀大;
猜想Ⅳ:铜绿加热产生一氧化碳和二氧化碳混合气体使气球胀大。
(实验与分析)①熄灭酒精灯后,气球依然胀大没有变瘪,证明猜想___________不成立。
②乙同学用下图装置进行实验:
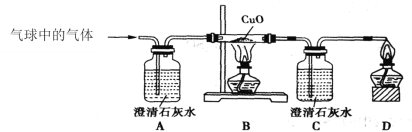
乙同学发现___________________,说明铜绿加热后有CO2产生,产生此现象的化学方程式是________,B处试管内的氧化铜没有变化,说明猜想___________不成立。
(实验结论)猜想Ⅱ成立。
(反思)
(1)加热铜绿反应的化学方程式是__________________。
(2)丙同学认为乙同学如果省略A可达到相同的结论,具体的操作是______________________。