题目内容
【题目】![]() 、
、![]() 、
、![]() 分别表示氢元素的三种原子,可简写成
分别表示氢元素的三种原子,可简写成![]() 、
、![]() 、
、![]() .制造燃料电池常用
.制造燃料电池常用![]() ,制造氢弹要用
,制造氢弹要用 ![]() 、
、![]() 。请据图回答:
。请据图回答:
(1)![]() 、
、![]() 、
、![]() 三种原子中,_______数目不等(填“质子”或“中子”或“电子”)。
三种原子中,_______数目不等(填“质子”或“中子”或“电子”)。
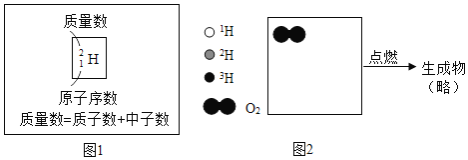
(2)![]() 与O2 反应生成的重水可表示为
与O2 反应生成的重水可表示为![]() .写出
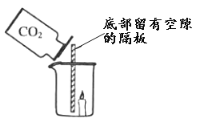
.写出![]() 在O2 中燃烧的化学方程式_______,在图 2 所示的小方框中,把
在O2 中燃烧的化学方程式_______,在图 2 所示的小方框中,把 ![]() 与 O2 恰好完全反应的反应物微观粒子补画齐全_______。
与 O2 恰好完全反应的反应物微观粒子补画齐全_______。
【答案】中子 23H2+O2![]() 23H2O
23H2O 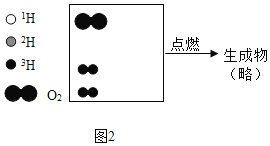
【解析】
(1)1H、2H、3H三种原子中,质子数和电子数相同,中子数目不等。
(2)由题意可知,3H2在O2中燃烧生成了3H2O,反应的化学方程式是:23H2+O![]() 223H2O,由质量守恒定律可知,每2个3H2与1个O2恰好反应,所以在小方框应补充2个3H2分子。如下图:
223H2O,由质量守恒定律可知,每2个3H2与1个O2恰好反应,所以在小方框应补充2个3H2分子。如下图:
故答为:(1)中子;(2)23H2+O2![]() 23H2O,见上图。
23H2O,见上图。

【题目】某化学兴趣小组用实验室常用药品(或溶液)对“NaOH溶液与稀盐酸是否恰好完全反应”进行探究。
(知识卡片):氯化钠溶液显中性。氯化铜易溶于水。
(实验探究):
(1)方案Ⅰ:某同学先向试管中加入约2mLNaOH溶液,再滴入几滴酚酞溶液,溶液变红。然后慢慢滴入稀盐酸,边滴边振荡,直至溶液恰好变为无色。
①实验结论_________。
②从微观的角度分析,该反应的实质是_________。
③在滴入稀盐酸的过程中,若观察到有少量气泡出现,请分析产生气泡的可能原因_______(用化学方程式表示)。
(2)方案Ⅱ:
实验步骤 | 实验现象 | 结论 |
取2mLNaOH溶液于试管中,滴入一定量的稀盐酸,振荡后加入镁条 | 若_______ | 稀盐酸过量 |
若没有明显现象 | NaOH溶液与稀盐酸恰好完全反应 |
(实验反思):
(3)另有同学提出方案Ⅱ不能证明NaOH溶液与稀盐酸恰好完全反应,其原因是______。
(4)除以上方案外,下列哪些物质单独使用,也能证明“NaOH 溶液与稀盐酸是否恰好完全反应”_________ (填序号)。
A 铜片 B pH试纸 C 氧化铜 D 紫色石蕊试液