题目内容
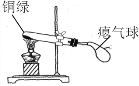
【题目】兴趣小组同学发现实验室一片久置的铜片表面附着有一层绿色固体,查阅资料得知绿色固体是铜绿 [化学式为Cu2(OH)2CO3],甲同学从铜片上刮下一些铜绿进行如下探究,请填写下表中空白:
实验步骤 | 实验现象 | 实验结论 |
| 试管内壁有水雾。 | 铜绿加热产生_________。 |
_________________。 | 铜绿加热后生成氧化铜。 | |
气球胀大。 |
乙同学对气球胀大产生兴趣,于是进行了如下的探究。
(发现问题) 气球为什么会胀大?
(提出猜想) 猜想Ⅰ:试管内的空气受热膨胀使气球胀大;
猜想Ⅱ:铜绿加热产生二氧化碳使气球胀大;
猜想Ⅲ:铜绿加热产生一氧化碳使气球胀大;
猜想Ⅳ:铜绿加热产生一氧化碳和二氧化碳混合气体使气球胀大。
(实验与分析)①熄灭酒精灯后,气球依然胀大没有变瘪,证明猜想___________不成立。
②乙同学用下图装置进行实验:
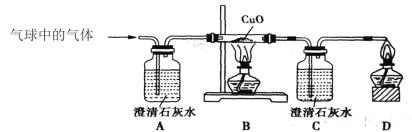
乙同学发现___________________,说明铜绿加热后有CO2产生,产生此现象的化学方程式是________,B处试管内的氧化铜没有变化,说明猜想___________不成立。
(实验结论)猜想Ⅱ成立。
(反思)
(1)加热铜绿反应的化学方程式是__________________。
(2)丙同学认为乙同学如果省略A可达到相同的结论,具体的操作是______________________。
【答案】水(或H 2O) 试管中的固体变黑色(或试管中有黑色固体出现) Ⅰ A中的澄清石灰水变浑浊 CO2 +Ca(OH)2=CaCO3↓+H2O Ⅳ Cu2(OH)2CO3![]() 2CuO+H2O+CO2↑ 先通入气体一会儿,后点燃B处酒精灯
2CuO+H2O+CO2↑ 先通入气体一会儿,后点燃B处酒精灯
【解析】
解:加热铜绿时,试管内壁有水雾,说明铜绿加热产生水;氧化铜是黑色固体,所以还观察到试管中的固体变黑色;
[实验与分析]①熄灭酒精灯后,气球依然胀大没有变瘪,证明不是试管内的空气受热膨胀使气球胀大,即猜想Ⅰ不成立;
②二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水,若铜绿加热后有CO2产生,则A中的澄清石灰水会变浑浊;B处试管内的氧化铜没有变化,说明原气体中不含一氧化碳,即猜想Ⅲ、Ⅳ均错误;
[反思](1)由实验现象可知,铜绿在加热的条件下生成氧化铜、水和二氧化碳,反应的化学方程式:Cu2(OH)2CO3![]() 2CuO+H2O+CO2↑;
2CuO+H2O+CO2↑;
(2)在实验中可先通入气体一会儿,后点燃B处酒精灯,若观察到C处澄清的石灰水变浑浊,B处的固体没有变化,也可得到相同的结论;故填:先通入气体一会儿,后点燃B处酒精灯。

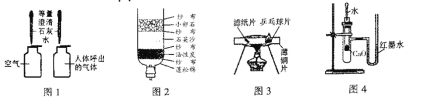
【题目】下列实验不能达到实验目的的是( )
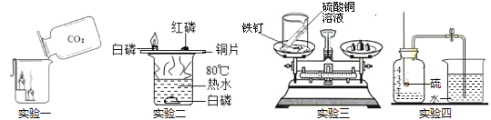
A. 实验一验证二氧化碳密度大于空气,不支持燃烧且不具备燃烧
B. 实验二探究燃烧需要的条件
C. 实验三探究质量守恒定律
D. 实验四测量空气中氧气所占的体积分数
【题目】某化学小组同学做镁条在空气中燃烧实验时,发现生成物中还有少量黑色固体,针对这一现象及相关问题,他们展开了如下探究,请仔细阅读并参与他们的探究之旅。
(探究目的)探究黑色固体时镁与空气中什么物质反应产生的?
(查阅资料)
(1)稀有气体一般不与其它物质反应;
(2)光亮的镁条与水反应,表面会生成白色固体。
(分析猜想)分析空气中各成分,进行猜想:
(1)猜想①是氧气 猜想②是氮气 猜想③是_____________。
(实验一)镁带与氧气的反应
(一)甲同学探究了影响过氧化氢制取氧气速度的某种因素,进行了三次实验并记录了各种收集相同体积氧气所需要的实验如下表:
实验 | 过氧化氢的浓度 | 过氧化氢溶液的质量(g) | 二氧化锰的质量(g) | 收集时间(s) |
1 | 10% | 20 | 1 | 40 |
2 | 15% | 20 | 1 | 20 |
3 | 20% | X | 1 | 12 |
(2)第3次实验中,X的值应为_______________;
(3)实验结论:在相同条件下,___________,过氧化氢分解得越快。
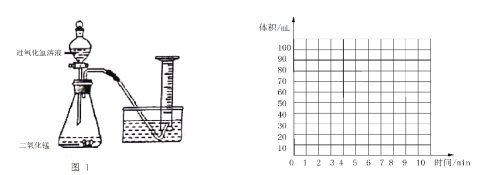
(二)乙同学在量筒中盛满水,倒置与水槽中,通过分液漏斗把20 mL某浓度得过氧化氢溶液加入锥形瓶中,记录量筒中气体得体积(图1)。数据如下表:
时间/min | 1 | 3 | 5 | 7 | 9 | 10 |
量筒读数/mL | 60.0 | 82.0 | 88 | 89.5 | 90 | 90 |
(4)请根据以上过程和实验数据综合分析,最终生成氧气得体积是_________mL;
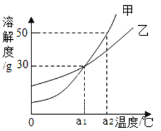
(5)请在下面坐标中绘制出0~10min生成氧气体积随时间变化得曲线____________;
(三)燃烧镁带,观察现象
将镁带打磨光亮,点燃,伸入盛满氧气的集气瓶中,产生大量白烟,生成白色固体。
实验结论:镁与氧气反应生成白色的氧化镁。
(实验二)镁带与氮气的反应
(一)收集纯净的氮气
(二)燃烧镁带,观察现象
将镁带打磨光亮,点燃,伸入盛有氮气的集气瓶中,瓶内壁附着一层淡黄色的固体。
(6)实验结论:镁与氮气在点燃得的条件下发生化合反应生成淡黄色的氮化镁(Mg3N2),该反应的化学方程式是______________。
(探究结论1)
(7)综上所述,关于镁在空气中燃烧产生黑色固体的猜想是猜想________(填序号)成立。
(探究结论2)
(8)如果用足量的镁替代红磷进行空气组成实验,实验测得氧气的体积分数比实际值_______(填“偏大”或“偏小”)。
(实验回顾)实验室常用红磷燃烧的方法测定空气中氧气含量(图2),由于红磷需要在瓶外点燃再伸入瓶内,常常带来污染以及误差。
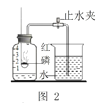
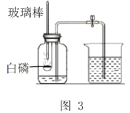
(实验改进)同学们选择了着火点更低的白磷,并对装置图做了改进(图3).主要操作是:再实际容积为180mL的集气瓶里,先装进50 mL的水,再按图连接好仪器,按下热的玻璃棒,白磷立即被点燃。
(9)白磷从燃烧到熄灭冷却的过程中,瓶内水面的变化是_______________;
(10)若实验中无误差,最终集气瓶中水的体积约为_________mL。
(11)集气瓶里预先装进50 mL水的作用,其一是为了加快集气瓶的冷却速度;其二则主要是_____。
(实验与交流)
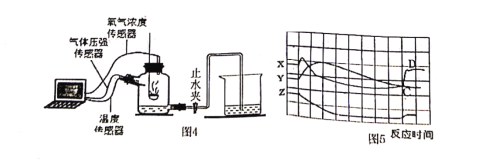
(12)为了帮助同学们更好地理解空气中氧气含量测定的实验原理,老师利用传感器技术定时测量了实验装置(图4)内的压强、温度和氧气浓度,三条曲线变化趋势如图5所示。Y曲线表示的是________(填“温度”或“氧气的浓度”或“压强”)变化趋势;X曲线中CD段上升的原因是________。
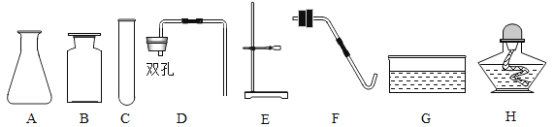
【题目】某化学活动兴趣小组用如图装置进行一氧化碳还原氧化铜的探究实验,反应一段时间后,玻璃管内黑色粉末全部变成红色,澄清石灰水变浑浊。
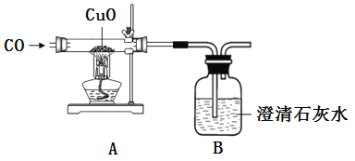
(1)从安全环保的角度考虑,上述实验需要改进的是______。
(2)装置A中发生反应的化学方程式为_____。
(3)同学们通过查阅资料得知:①氧化亚铜(Cu2O)和铜均为红色固体;②铜不与稀硫酸反应,Cu2O能和稀硫酸反应(化学方程式为Cu2O+H2SO4=CuSO4+Cu+H2O);③硫酸铜溶液为蓝色。他们对反应后玻璃管中的红色固体进行如下探究:
(提出问题)反应后生成的红色固体成分是什么?
(作出猜想)猜想一:红色固体只有Cu
猜想二:红色固体只有Cu2O
猜想三:红色固体为______。
(实验探究)设计如下实验方案
实验操作 | 现象 | 结论 |
甲同学取少量红色固体于试管中, 加入过量的稀硫酸。 | _________ | 猜想一正确。 |
乙同学另取少量红色固体于试管中,加入过量的稀硫酸。 | 溶液变蓝色,有红色固体剩余。 | 猜想二正确。 |
(思考与分析)乙同学认为猜想二正确,同学们分析后认为他的结论不准确,理由是________。为此,同学们补充进行了以下实验:称取mg红色固体于试管中,加入过量的稀硫酸充分反应,然后过滤、洗涤、干燥、称量,得到ng固体。当n>______(含m的代数式)时,可以得出猜想三的结论正确。