��Ŀ����
����������۲졢ѧϰ����һ��ʵ�顣ȡ�Ķ���ʯ����ҺȾ����ɫ�ĸ����ֽ�����ֱ���ͼ����ʵ�顣
�����ͼʾ����˼�����ش��±��е����⣺
| | ��I�� | ��II�� | ��III�� | ��IV�� |
| ���� | ��ɫֽ����� | ��ɫֽ������ɫ | ��ɫֽ������ɫ | ______ ______ |
| ���� | ��ʵ��(III)��֤�� �� ʵ��(��)��֤�� �� ��ͨ��ʵ��(I)��(��)������֤���һ����ѧ������ �� ��ʵ��(��)������ֽ���þƾ���С�ļ��Ⱥ濾��ֽ���ֱ��ϣ� ˵��̼�� ����д�����ֱ���ʽ | |||
(��)����ɫֽ�����ɫ�� ��(��)��������̼����ʹ��ɫʯ���죻 (��)��ˮ�Ͷ�����̼��ͬ����ʹ��ɫʯ����(��̼��ʹ��ɫʯ����Һ���)�� ������ʹ��ɫʯ����Һ��졣 �ۻ�ѧ���ʲ��ȶ��������ֽ⡣ ̼�� ˮ+������̼
���������������ϡ������ɫֽ����죬˵������ʹ��ɫʯ����Һ��ɫ����ˮ��ɫֽ������ɫ��˵��ˮ����ʹ��ɫʯ����Һ��ɫ��ֱ�ӷ������Ķ�����̼����ɫֽ������ɫ��˵��������̼����ʹ��ɫʯ����Һ��ɫ[������ˮ����� ������̼����ɫֽ����ɫ��˵��������̼��ˮ��Ӧ�������ᣬ��ʹ��ɫʯ����Һ��ɫ��������̼��ˮ��Ӧ���ɵ�����̼�ᣬ̼��ȶ��������ֽ⡣
���㣺������̼�Ļ�ѧ����

 ���Ǽ���С����ϵ�д�
���Ǽ���С����ϵ�д� �Ͻ�ƽ���Ȿϵ�д�
�Ͻ�ƽ���Ȿϵ�д������װ�г�ʹ��һ�ִ�װ��������Ʒ��Ϊ��504˫�����������ǩ����ͼ��ʾ��ͬѧ�Ƕ�һ�����õġ�504˫������������Ʒ�ܺ��棬���ʵ�����̽����
��������⡿���ù���ijɷ���ʲô��
���������ϡ������Ȼ�����Һ�ڳ����·�����Ӧ�����Ȼ�������
���������롿���ù����п��ܺ���Fe��Fe2O3��CaO��Ca(OH)2��CaCO3�����ù����п��ܺ���Ca(OH)2��ԭ���ǣ��û�ѧ����ʽ��ʾ���� ����
��ʵ��̽��1��
��ͬѧ�ķ�����
| ʵ����� | ʵ������ | ʵ����� |
| ��1��ȡ������������Թ��У�����������ˮ�ܽ⣬���ú�ȡ�ϲ���Һ�μ���ɫ��̪��Һ | �����ܽ�ʱ�Թ���ڷ��̣��Թܵײ��в������Һ��졣 | ������һ�������� �� ���������ơ� |
| ��2����ȡ������������Թ��У��μ��������� ���� | ��������ʧ���д�����ɫ����������õ�dz��ɫ��Һ�� | ������һ�������� ���� һ������Fe2O3 |
| ��3�������裨2���в���������ͨ�뵽�����ʯ��ˮ�� | �� �� | ������һ������CaCO3 |
��1����ͬѧ��Ϊ��ͬѧ��ʵ���в��ܵó�һ����Ca(OH)2�Ľ��ۣ��������� ����
��2����ͬѧ��Ϊ��ͬѧ��ʵ�鲢���ܵó�һ������Fe2O3�Ľ��ۣ��������� ����
��ʵ��̽��2��
�ҡ���ͬѧ�������ʵ�鷽��������֤��
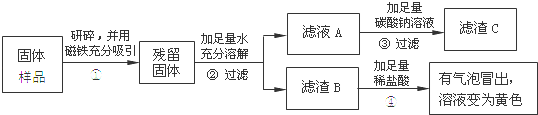
��1�����з�Ӧ�Ļ�ѧ����ʽ���� ����
��2���ҡ���ͬѧʵ�������ܵó�������Ʒ��һ���������� ��������һ�����ʲ���ȷ�������������� ����
��3���ҡ���ͬѧ�־���ʵ�����������������к������ʵ�������Ϊ1.6g������B��CaCO3������Ϊ1.0g������C������Ϊ1.0g��
��ʵ����ۡ��ۺ�����ʵ�鼰�������ݣ����ù���ijɷ����� ����

����ʦ��ָ���£�ͬѧ�ǽ�������Ȥ�Ļ�ѧʵ��̽����
һ���ⶨ��������������
ͼ1��ʾ����С��ͬѧ�ú����ڿ�����ȼ�յIJⶨ�����������ǣ�
��1����������ƿ�ݻ�����Ϊ��ȷݣ������ñ�ǣ�
��2������ȼȼ�ճ��ڵĺ��ף����뼯��ƿ�в�������������
��3����������Ϩ����ȴ���ɼУ�����ˮ�����뼯��ƿ�У����뼯��ƿ��ˮ�����ԼΪ����ƿ���ݻ���1/5����ش��������⣺

�ٵ�2������ȼ��ʱ������ ��
��ѧ��Ӧ����ʽ�� ��
��ʵ����ϣ������뼯��ƿ��ˮ������������ݻ���1/5��
����Ϊ������һ�����ԭ������� ��
A������ƿ�ײ���ˮռ��һ�������
B��������
C������û��ȼ����ͼ��Ŵ���ֹˮ��
��С��ͬѧ��ʵ����з�˼������˸Ľ���������ͼ2��ʾ����С������ʽ��ʼʵ��ǰ���н����ɼУ���ע����������20mL�̶ȴ�����15mL����Ȼ���ɿ��������۲쵽����������20mL�̶ȴ����ò�������ҪĿ���� ������Ϊ�Ľ�����ŵ��� ��
����С���Ķ��������ϵ�֪��˫��ˮ�ֽ�����ö������̣�MnO2������������ͭ��CuO����������������������������ͭ������̽����Ȥ��
��������⡿����ͭ�Ƿ�Ҳ��������طֽ�Ĵ��������Ƿ�ȶ������̴�Ч�����ã�
�����ʵ�顿С�������ɵ����������Ϊ�����������������ʵ�飨��������Ӱ��ʵ��
�����ؾ����ԣ�
| ʵ����� | ��������� | ������������ | �������� |
| �� | 1.2g | / | |
| �� | 1.2g | CuO 0.5g | |
| �� | 1.2g | MnO2 0.5g | |
������ʵ��Ӧ�����ġ��������ݡ��� ��
����ʵ��ڱ�ʵ��ٵġ��������ݡ��� (���С��)��˵������ͭ�ܼӿ�����صķֽ⡣
�۽�ʵ��ڷ�Ӧʣ��Ĺ���ȡ����ϴ�ӡ�����ٴξ�ȷ�����õ�0.5g��ɫ��ĩ����������Ŀ���� ��С��ͬѧ��Ϊ����ͭ�϶�������طֽ�Ĵ�������С��ͬѧ�Դ���������飬С��ͬѧ���������ʵ�飺
���ڶ��ξ�ȷ�����õ���0.5g��ɫ��ĩ��1.2g����ػ�Ϸ����Թ��У����ȣ����������ľ��������ľ���ܿ츴ȼ��
С��ͬѧ������Ŀ���� ��
��Ԥ�ڽ��ۡ�����ͭҲ��������صĴ�����
��������ơ�����ΪС�����ʵ��ۺ�ʵ��ڶԱȵ�Ŀ���� ��д��ʵ��ڷ�Ӧ�ı���ʽ ��
������Ȥ�ĸĽ�ʵ��
��С��ͬѧѧ�˷�������������ݺĽ����鱾��̽�������˶���ʵ�顣С��ͬѧ����������ҽ����Ʒ-----��Y �ιܣ������ͼ1��ʾʵ�飬�����и�ʵ����Ϊ��̽�� ��ʵ��������ܿ����������� ��С��ͬѧ��Ƶ�ʵ���ŵ��� ��
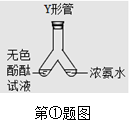
��������ͼװ�ý��С���ȼ�ա���ʵ�飺�����䣨�ܲ��Ϲ��������װ�ã����ϵ������;�֧�Թ��й��������ͬʱ�þƾ��Ƹ���ۼ�����ȼ�գ���ȥ�ƾ��ƣ��ɹ۲쵽���ĵ���ɫ���棻Ȼ��ֹͣ������������þƾ��Ƹ�������ؼ��ȣ�ʹ���ڴ����м���ȼ�գ��۲쵽�� �����档
д��ʵ�������ȼ�յĻ�ѧ��Ӧ����ʽ�� ����ʵ��װ�õ���Ҫ�ŵ����������к�����Ի�����Ⱦ��ǰ������������ �������ƶ��ձ��е�����������Һ�� ������ ��

Ϊ���ij�������ŷŵķ�Һ���Ƿ���SO42-��ͬѧ����������·�������������ʵ�顣
| ���� | ���� | ���� | ���� |
| �� | ��ȡ��Ʒ���μ�BaCl2��Һ �ڶԲ���ٷ�Ӧ��Ļ������й��ˣ��������еμ�ϡ���� | ���а�ɫ�������� ������������ | ��Һ�к���SO42�� |
| �� | ��ȡ��Ʒ���μӹ���_____________�� ���ڲ���ٵ���Һ�еμ�BaCl2��Һ | ������������ ���а�ɫ�������� | ��Һ�к���SO42- |
| �� | ��ȡ��Ʒ���μ�Ba��NO3��2��Һ �ڶԲ���ٲ����Ļ������й��ˣ��������еμ�ϡ���� | ���а�ɫ�������� ������������ | ��Һ�к���SO42- |
��1���������ʵ����������ȷ��������еμӵ��������� ����21���ͽ�����
��2��������͢��У����۲������ķ������� ���������� ����
��3��������������У��μ�ϡ������Ϊ���ų��� �ĸ��š�
����ͬѧ�ڻ�ѧʵ���ҷ���һƿʢ����ɫ��Һ���Լ�ƿ�����ǩ����������ͼ��ʾ������ʦ����������ƿ�Լ����������ᡢ�����ơ�����ͭ������þ��Һ�е�һ�֣�[��������]���������������ʵ��ܽ�����±���
| ���� | H2SO4 | Na2SO4 | MgSO4 | CuSO4 |
| �ܽ��/g | ��ˮ����Ȼ��� | 19.0 | 39.0 | 23.1 |
��2��Ϊȷ����ɷ�����ͬѧ�Դ���Һ��������ʵ��̽����
[��������]����Һ������ ��Һ��
[ʵ����֤]
| ʵ�鷽�������� | ���ܳ��ֵ����� | ���ۻ��йػ�ѧ����ʽ |
| | | |
Ϊ��һ���о�������صķֽ���ij��ȤС��ͬѧ�������ϣ���ȡһ�������ĸ�����ؼ���ʹ֮��ȫ�ֽ⣬Ȼ��ֱ��������������ʵ�顣
��ʵ�����ݡ���
| ��� | ʵ������ | ʵ������ | ʵ����� |
| 1 | ȡ��Ӧ�����ʣ����0.2g����5mL 6%��H2O2��Һ�� | ���ҷ�Ӧ���ų����������������������� | ����ʣ�����е�MnO2��H2O2�ֽ��д����� |
| 2 | ȡ0.2gMnO2����5mL a ��H2O2��Һ��������������H2O2��Һ�� | ƽ�ȷ�Ӧ���ų������������������� | MnO2��H2O2�ֽ��д����� |
| 3 | ȡ��Ӧ�����ʣ����1.0g��������ˮ�У�����ܽ⣬���� | ������ȫ�ܽ⣬��ֽ����ɫ��������� | ����ʣ�������� b |
��ʵ�������
��1������ϱ��е�������ݣ�a ��b ��
��2��ʵ��2��Ŀ���� ��
��3��ͬѧ�Ǿ������ۣ���Ϊʵ��1�Ľ��۲���ȷ�������� ��
���������ϡ�
��KMnO4���ȷֽ�ʱ����ij�����¿��ܷ�������������Ӧ��
��6KMnO4
 2K2MnO4+K2Mn4O8+4O2��
2K2MnO4+K2Mn4O8+4O2�� ��KMnO4
 KMnO2+O2��
KMnO2+O2������Է�����������KMnO4��158 O2��32��
��4��16gKMnO4����Ԫ�ص�����Ϊ ������ʹ֮��ȫ�ֽ⣬����ȫ������Ӧ�٣�����O2������Ϊ ����ͬʱ������Ӧ�٢ڣ�����O2��������Χ�� ����������λС������ʾ�����������غ㶨�ɹ۲죩
ij�о���ѧϰС��ѡ��H2O2����O2�Ŀ�����ʲô�����йء��Ŀ������̽��������������̽������Ҫ���̣�
[����] H2O2����O2�Ŀ�������������й�
[ʵ�鷽��]�����£�����ƿ��ͬ�����H2O2��Һ�зֱ������ͬ����MnO2�ͺ�ש�ۣ�����������һƿ����ͬ�����O2�����ʱ�䡣
[�����¼]
| ������ | 1 | 2 |
| ��Ӧ�� | 6% H2O2 | 6% H2O2 |
| ���� | 1g��ש | 1gMnO2 |
| ʱ��(��) | 152 S | 35 S |
[����]
��̽�����̵ó��Ľ����� ��
[��˼]һ����Ա˵����ʵ�黹����֤����ש�ۿ������÷�Ӧ�Ĵ�������Ҫ֤����ש���Ǹ÷�Ӧ�Ĵ���������Ҫ������������֤��������Ϊ��Ҫ���ӵ�ʵ����֤�������ڻ�ѧ��Ӧǰ��� ��_____ �Ƿ�ı䡣
[��չ]H2O2����O2�Ŀ���������Щ�����йأ�
[����]

